- Авторы
- Резюме
- Файлы
- Ключевые слова
- Литература
Сизова Ю.В. 1 Писанов Р.В. 1 Водопьянов А.С. 1 Черепахина И.Я. 1 Бурлакова О.С. 1 1 ФКУЗ «Ростовский-на-Дону противочумный институт» Роспотребнадзора С появлением генетически измененных вариантов холерных вибрионов возник вопрос о диапазоне вариабельности фенотипических и генотипических проявлений токсинопродукции у типичных и атипичных по генотипу вариантов холерных вибрионов. С учетом актуальности проблемы проведены опыты по оценке влияния стрессовых условий, с которыми вибрионы сталкиваются в окружающей среде, на способность к продукции холерогена. В результате проведенных исследований было показано, что токсигенные холерные вибрионы могут сохраняться в воде открытых водоемов при температуре 220С-240С достаточно продолжительный срок с сохранением продукции холерного токсина, при понижении температуры до 100С и ниже уровни токсинопродукции снижаются вплоть до отрицательных значений. Установлено, что гены ctхAB обнаруживаются в ПЦР до тех пор, пока в популяции исследуемых штаммов сохраняются живые вибрионы, при этом изменений в популяции клеток вибрионов, связанных с утратой профага CTXφ, а также других значимых участков генома после низкотемпературного стресса в наших экспериментах не отмечено, что подтверждается в полногеномном секвенировании и INDEL-типировании исходных и стрессированных культур и говорит о стабильности генома холерных вибрионов в указанных условиях.  438 KB атипичные штаммы холерный вибрион токсинопродукция 1. Водопьянов А.С. INDEL-и VNTR-типирование штаммов Vibrio cholerae, выделенных в 2013 году из объектов окружающей среды на территории Российской Федерации / А.С. Водопьянов, С.О. Водопьянов, И.П. Олейников, Б.Н. Мишанькин, В.Д. Кругликов, И.В. Архангельская, Д.А. Зубкова, М.И. Ежова // ЗНиСО. – 2015. – № 5 (266). – С. 41-44. 2. Водопьянов С.О. Испытание метода ПЦР в работе индикационной лаборатории мобильного комплекса СПЭБ при исследовании экспериментальных проб на холеру/ С.О. Водопьянов, А.С. Водопьянов, И.П. Олейников, Р.В. Писанов, А.Б. Мазрухо // ЗНиСо. – 2011. – № 8. – С.43-45. 3. Заднова С.П. Изменение свойств штаммов холерного вибриона классического биовара под действием факторов внешней среды и мобильных генетических элементов / С.П. Заднова, Н.Д. Исаев, Ю.В. Лозовский, Н.И. Смирнова // Холера и патоген. для чел-ка вибр.: Матер. совещ. и пробл. комис. – Ростов-на-Дону, 2007. – Вып. 20. – С. 102–105. 4. Кульшань Т.А. Сравнительный анализ участков генома, связанных с вирулентностью, у природных штаммов Vibrio cholerae классического и Эль Тор-биоваров / Т.А. Кульшань, Н.Б. Челдышова, Н.П. Гусева, Н.И.Смирнова // Эпидемиология и инфекционные болезни. – 2014. – № 2. – С.26-33. 5. Кульшань Т.А. Оценка функциональных особенностей и стрессоустойчивости изогенных токсигенных и нетоксигенных штаммов Vibrio cholerae биовара Эль Тор / Т.А. Кульшань, С.П. Заднова, Н.Б. Челдышова, Н.И. Смирнова // Журн. микробиол., эпидем. и иммунобиол. – 2015. – № 3. – С. 11–17. 6. Методические указания (МУ) 1.3.2569-09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I–IV групп патогенности» . – URL: http://lawru.info/dok/2009/12/22/n229579.htm (дата обращения: 25.04.2017 г.). 7. Миронова Л.В. Анализ стабильности генома Vibrio cholerae в условиях низкой температуры и дефицита питательных веществ / Л.В. Миронова, Ж.Ю. Хунхеева, Е.А. Басов, А.С. Пономарева, С.К. Миткеева, С.В. Балахонов // Проблемы ООИ. – 2016. – № 3. – С.52-56. 8. Писанов Р.В., Симакова Д.И. Роль малых рнк в контроле экспрессии генов, вовлеченных в реализацию патогенности Vibriocholerae / Р.В. Писанов, Д.И. Симакова // Холера и патоген. для чел-ка вибр.: Матер. совещ. и пробл. комис. – Ростов-на-Дону, 2016. – Вып. – С. 136-139. 9. Сизова Ю.В. Влияние температуры на токсинопродукцию холерных вибрионов в речной воде / Ю.В. Сизова, О.С. Бурлакова, И.Я. Черепахина, Л.П. Алексеева, В.В. Евдокимова, Р.В. Писанов, С.О. Водопьянов // ЗНиСО. – 2016. – № 6. – С. 54-56. 10. Смирнова Н.И. Эволюция возбудителя холеры / Н.И. Смирнова, В.В. Кутырев // Молекулярная генетика, микробиология и вирусология. – 2004. – 4. – С.3–13. 11. Faruque S.M. Pathogenicity island and phages in Vibrio cholerae evolution / S.M. Faruque, J.J. Mekalanos // Trends. Microdiol. – 2003. – V.11(11). – P.505-510. 12. Iwanaga M. Culture conditions for stimulating cholera toxin production by Vibrio cholerae O1 El Tor /M. Iwanaga, K. Yamamoto, N. Higa // Microbiol. Immunol. – 1986. – Vol.30. – Р.1075–83. 13. Mutreja A. Evidence for several waves of global transmission in the seventh cholera pandemic / A. Mutreja, D.W. Kim, N.R. Thomson, Т.R. Connor et al. // Nature. – 2011. – Р. 462–465. 14. Safa, A. Evolution of new variants of Vibrio cholerae O1 /A. Safa, G.B. Nair, R.Y. Kong // Trends Microbiol. – 2010. – V. 18. – P. 46-54. 15. Zerbino D.R., Birney E. Velvet: algorithms for de novo short read assembly using de Bruijn graphs / D.R. Zerbino, E. Birney // Genome Research. – 2008. – Т. 18. – №. 5. – С. 821-829.
438 KB атипичные штаммы холерный вибрион токсинопродукция 1. Водопьянов А.С. INDEL-и VNTR-типирование штаммов Vibrio cholerae, выделенных в 2013 году из объектов окружающей среды на территории Российской Федерации / А.С. Водопьянов, С.О. Водопьянов, И.П. Олейников, Б.Н. Мишанькин, В.Д. Кругликов, И.В. Архангельская, Д.А. Зубкова, М.И. Ежова // ЗНиСО. – 2015. – № 5 (266). – С. 41-44. 2. Водопьянов С.О. Испытание метода ПЦР в работе индикационной лаборатории мобильного комплекса СПЭБ при исследовании экспериментальных проб на холеру/ С.О. Водопьянов, А.С. Водопьянов, И.П. Олейников, Р.В. Писанов, А.Б. Мазрухо // ЗНиСо. – 2011. – № 8. – С.43-45. 3. Заднова С.П. Изменение свойств штаммов холерного вибриона классического биовара под действием факторов внешней среды и мобильных генетических элементов / С.П. Заднова, Н.Д. Исаев, Ю.В. Лозовский, Н.И. Смирнова // Холера и патоген. для чел-ка вибр.: Матер. совещ. и пробл. комис. – Ростов-на-Дону, 2007. – Вып. 20. – С. 102–105. 4. Кульшань Т.А. Сравнительный анализ участков генома, связанных с вирулентностью, у природных штаммов Vibrio cholerae классического и Эль Тор-биоваров / Т.А. Кульшань, Н.Б. Челдышова, Н.П. Гусева, Н.И.Смирнова // Эпидемиология и инфекционные болезни. – 2014. – № 2. – С.26-33. 5. Кульшань Т.А. Оценка функциональных особенностей и стрессоустойчивости изогенных токсигенных и нетоксигенных штаммов Vibrio cholerae биовара Эль Тор / Т.А. Кульшань, С.П. Заднова, Н.Б. Челдышова, Н.И. Смирнова // Журн. микробиол., эпидем. и иммунобиол. – 2015. – № 3. – С. 11–17. 6. Методические указания (МУ) 1.3.2569-09 «Организация работы лабораторий, использующих методы амплификации нуклеиновых кислот при работе с материалом, содержащим микроорганизмы I–IV групп патогенности» . – URL: http://lawru.info/dok/2009/12/22/n229579.htm (дата обращения: 25.04.2017 г.). 7. Миронова Л.В. Анализ стабильности генома Vibrio cholerae в условиях низкой температуры и дефицита питательных веществ / Л.В. Миронова, Ж.Ю. Хунхеева, Е.А. Басов, А.С. Пономарева, С.К. Миткеева, С.В. Балахонов // Проблемы ООИ. – 2016. – № 3. – С.52-56. 8. Писанов Р.В., Симакова Д.И. Роль малых рнк в контроле экспрессии генов, вовлеченных в реализацию патогенности Vibriocholerae / Р.В. Писанов, Д.И. Симакова // Холера и патоген. для чел-ка вибр.: Матер. совещ. и пробл. комис. – Ростов-на-Дону, 2016. – Вып. – С. 136-139. 9. Сизова Ю.В. Влияние температуры на токсинопродукцию холерных вибрионов в речной воде / Ю.В. Сизова, О.С. Бурлакова, И.Я. Черепахина, Л.П. Алексеева, В.В. Евдокимова, Р.В. Писанов, С.О. Водопьянов // ЗНиСО. – 2016. – № 6. – С. 54-56. 10. Смирнова Н.И. Эволюция возбудителя холеры / Н.И. Смирнова, В.В. Кутырев // Молекулярная генетика, микробиология и вирусология. – 2004. – 4. – С.3–13. 11. Faruque S.M. Pathogenicity island and phages in Vibrio cholerae evolution / S.M. Faruque, J.J. Mekalanos // Trends. Microdiol. – 2003. – V.11(11). – P.505-510. 12. Iwanaga M. Culture conditions for stimulating cholera toxin production by Vibrio cholerae O1 El Tor /M. Iwanaga, K. Yamamoto, N. Higa // Microbiol. Immunol. – 1986. – Vol.30. – Р.1075–83. 13. Mutreja A. Evidence for several waves of global transmission in the seventh cholera pandemic / A. Mutreja, D.W. Kim, N.R. Thomson, Т.R. Connor et al. // Nature. – 2011. – Р. 462–465. 14. Safa, A. Evolution of new variants of Vibrio cholerae O1 /A. Safa, G.B. Nair, R.Y. Kong // Trends Microbiol. – 2010. – V. 18. – P. 46-54. 15. Zerbino D.R., Birney E. Velvet: algorithms for de novo short read assembly using de Bruijn graphs / D.R. Zerbino, E. Birney // Genome Research. – 2008. – Т. 18. – №. 5. – С. 821-829.
С учетом изменений условий существования холерных вибрионов при смене экологической ниши обитания вопрос о стабильности их генома в условиях стресса остается в настоящее время весьма актуальным, особенно в области признаков, касающихся эпидемической значимости возбудителя холеры. Установлено, что вся эволюция V.cholerae обеспечивается присутствием в геноме мобильных генетических элементов: профагов (CTXφ, RS1φ), островов пандемичности (VSP-I и VSP-II) и патогенности (VPI-1 и VPI-2), а также транспозонов и IS-элементов . Благодаря данным структурам, в конце прошлого столетия появились генетически измененные варианты V. cholerae биовара Эль Тор с повышенной вирулентностью (так называемые «гибридные» или «атипичные»), несущие в своем геноме ген ctxB1, присущий холерным вибрионам классического биовара. Такие вибрионы с 2001 г. полностью вытеснили типичные штаммы V.cholerae биовара Эль Тор на территории ряда стран Южной Азии (Непал, Индия, Бангладеш, Шри Ланка) и Африки (Мозамбик, Нигерия, Камерун). В 1994 году «атипичные» («гибридные») штаммы вызвали эпидемию холеры в Дагестане, а в 2010–2011 гг. – на о. Гаити . Однако, несмотря на высокую адаптивную способность холерных вибрионов, не решен вопрос: какие условия требуются для появления и закрепления изменений в геноме возбудителя. Между тем такие сведения крайне необходимы для оптимизации эпидемиологического надзора.
Цель исследования: изучение влияния ряда стрессоров, действию которых вибрионы подвергаются в окружающей среде, на токсинопродукцию.
Материалы и методы: в работе использовали 13 эпидемически значимых штаммов V.cholerae О1 серогруппы биовара Эль Тор (3 – типичные: ctxAB3, rstRElTor, 10 – атипичные: ctxAB1, rstRElTor) и 2 штамма классического биовара, содержащих гены ctxAB1, rstRClass.
Для решения поставленных задач холерные вибрионы инкубировали в стерильной речной воде (конечная концентрация 1*107 м.к./мл) при +40С и при +220С в течение нескольких месяцев, а также (при моделировании условий пребывания возбудителя холеры в речной воде в летнее, осеннее, зимнее время) эксперимент продолжали 2 месяца при 22 0С, 2 месяца – при 10 0С, 5 месяцев – при 4 0С при сниженном содержании кислорода (в речной воде оно составляет около 1 %). Ежемесячно производили высевы на агар Мартена для определения выживаемости холерных вибрионов. Выжившие в условиях стресса клетки культивировали по методике М. Iwanaga для определения продукции холерогена в супернатантах в GM1-ИФА с антитоксической сывороткой, полученной путем иммунизации кроликов по специально разработанной нами схеме, в рабочем разведении 1х20000. Результаты оценивали при титрации супернатантов по следующей схеме: низкий уровень токсинопродукции – титр в GM1-ИФА 1/2-1/20, средний уровень – 1/40-1/320, высокий уровень – 1/640-1/2560.
Выделение бактериальной ДНК из клеток V. cholerae проводили, согласно МУ 1.3.2569-09 . Полученные образцы, содержащие тотальную ДНК холерного вибриона, использовали для амплификации фрагментов генов. Наличие гена ctxAB определяли в ПЦР. Секвенирование геномной ДНК выполнялись на платформе MiSeq (Illumina). Пробоподготовку проводили согласно протоколам производителя. Сборку контигов осуществляли с помощью программы Velvet . Биоинформационный анализ проводили с помощью программ GeneExpert и SeqAnalyzer, разработанных во ФКУЗ «Ростовский-на-Дону противочумный институт» Роспотребнадзора с использованием ресурсов геномной базы данных NCBI.INDEL-типирование проводили по методике, предложенной А.С. Водопьяновым .
Результаты и обсуждение. Как нами было показано ранее , у холерных вибрионов при +4ºС в речной воде в течение первых 14 дней имеет место некоторое увеличение показателей токсинопродукции у большей части исследуемых штаммов (за исключением штаммов V.cholerae 1601 и 17427 – у них отмечалось незначительное снижение титра, и штаммов 569, 1310, 19188, у которых уровень продукции оставался без изменений). Однако уже через месяц стрессового воздействия показатели токсинообразования резко снижались, вплоть до полного исчезновения фенотипического проявления признака к концу второго месяца. Только три штамма V.cholerae ElTor сохраняли способность к токсинопродукции, определяемой методом ИФА: высокотоксигенный типичный 1310, типичный 3119 и атипичный 19667, выделенный от больного в Москве в 2014 г. Остальные 10 штаммов перестали продуцировать холероген, при сохранении генов ctxАВ, определяемых в ПЦР. Через три месяца низкотемпературного стресса ни одна из культур не выросла в среде AKI, показатели токсинопродукции были отрицательными, гены ctxAB в ПЦР не обнаружены.
Обращает на себя внимание, что реакция на стрессовое воздействие разных температур, имитирующих условия пребывания холерных вибрионов в речной воде, отличалась у типичных и атипичных вариантов. Так, средние показатели токсинопродукции при холодовом стрессе (4°С) у атипичных вариантов были выше только в первые две недели (рис. 1), затем уровень холерогена у них снижался интенсивнее, чем у типичных штаммов (показания высокотоксигенного исходного мутантного штамма 1310 в расчет не принимались), т.е. они были более чувствительны к низким температурам, чем типичные.
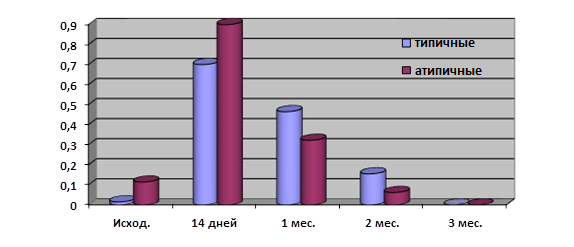
Рис. 1. Средние показатели токсинопродукции при длительной инкубации типичных и атипичных холерных вибрионов в речной воде при 4°С
Напротив, в отсутствие температурного стресса (22°С) средние показатели токсинопродукции у атипичных вариантов вибрионов Эль Тор на всем протяжении исследования были в 2–8 раз выше, чем у типичных штаммов, что в полной мере характеризует их, как варианты с повышенной вирулентностью (рис. 2).
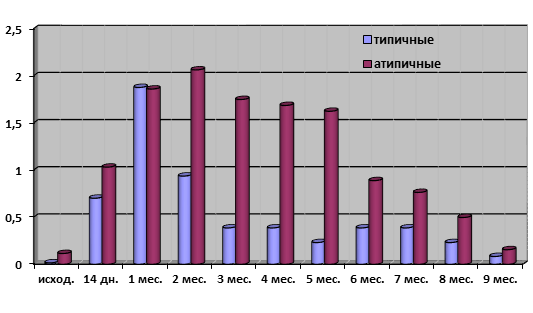
Рис. 2. Средние показатели токсинопродукции при длительной инкубации типичных и атипичных холерных вибрионов в речной воде при 22°С
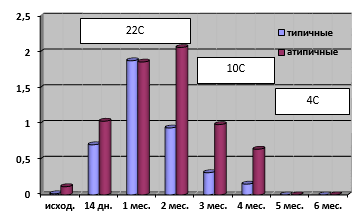
Рис. 3. Средние показатели токсинопродукции при длительной инкубации типичных и атипичных холерных вибрионов в речной воде при постепенной смене температур
При моделировании условий пребывания холерных вибрионов в водоемах Российской Федерации, в которых на протяжении эпидемического сезона температура постепенно снижается, токсинопродукция к 5 месяцу инкубации практически отсутствовала, но на протяжении 4 летне-осенних месяцев при 22°С и 10°С она в среднем в 2–4 раза была выше у атипичных вариантов (рис. 3), что необходимо учитывать при проведении эпиднадзора за холерой. Проведенные исследования показали, что фенотип возбудителя холеры в части токсинопродукции выраженно «отвечает» на стрессовые воздействия окружающей среды.
Что касается структуры генома, то в эксперименте Т.А. Кульшань с соавторами была показана возможность утраты генов профага СТХφ, в том случае, когда исследуемые «типичные» штаммы холерных вибрионов несли одну копию профага, в то время как атипичные «гибридные» геноварианты с двумя копиями профага СТХφ сохраняли указанные гены . В наших опытах в ПЦР отмечено сохранение генов патогенности вне зависимости от отрицательных показателей ИФА, до тех пор, пока в популяции исследуемых штаммов сохранялись живые вибрионы. В «пустых» пробах, исследуемых после гибели всей популяции V.cholerae, гены, ответственные за токсинопродукцию, не обнаруживались.
В свете полученных данных представляло интерес сравнить геномы исходных и стрессированных вариантов холерных вибрионов, для чего было проведено полногеномное секвенирование 3 штаммов, а также сравнение их INDEL-профилей по 9 локусам (табл.1,2).
В таблице 1 представлены результаты сиквенса, выраженные в процентах совпадения с референс-последовательностью.
Таблица 1
Результаты полногеномного секвенирования исходных и стрессированных культур холерных вибрионов
|
Анализируемые гены |
19241 (301) морская вода, 2011г |
больной, 1972г |
V.cholerae classical больной, 1968 |
||||
|
исходный |
стресс |
исходный |
стресс |
исходный |
стресс |
||
|
Принадлежность к виду V. cholerae |
ompW (VCA0867) |
100,00 |
100,00 |
100,00 |
100,00 |
99,16 |
99,16 |
|
Коллагеназа(VC1650) |
99,74 |
99,70 |
99,80 |
99,80 |
99,21 |
99,21 |
|
|
100,00 |
100,00 |
100,00 |
100,00 |
98,1 |
98,1 |
||
|
Серогруппа |
О1 (ген wbe) |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
|
Биовары |
hlyA Eltor |
100,00 |
100,00 |
100,00 |
100,00 |
98,9 |
98,9 |
|
hlyA classical |
94,6 |
94,6 |
97,6 |
97,6 |
100,00 |
100,00 |
|
|
rtxCElTor(VC1450) |
100,00 |
100,00 |
100,00 |
100,00 |
|||
|
Профаг CTX |
cep (VC1461) |
100,00 |
100,00 |
100,00 |
100,00 |
98,00 |
98,00 |
|
orfU (VC1460) |
100,00 |
100,00 |
100,00 |
100,00 |
96,1 |
96,1 |
|
|
ace (VC1459) |
100,00 |
100,00 |
100,00 |
100,00 |
98,6 |
98,6 |
|
|
zot (VC1458) |
100,00 |
100,00 |
100,00 |
100,00 |
98,8 |
98,8 |
|
|
ctxA (VC1457) |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
|
|
ctxB1 (Classical) |
100,00 |
100,00 |
100,00 |
100,00 |
99,47 |
99,47 |
|
|
ctxB3 (El Tor) |
99,47 |
99,47 |
100,00 |
100,00 |
|||
|
Профаг RSI |
RstR (VC1464) |
100,00 |
100,00 |
100,00 |
100,00 |
||
|
RstA (VC1454) |
99,63 |
100,00 |
98,81 |
98,81 |
98,8 |
98,8 |
|
|
rstС (VC1452) |
100,00 |
100,00 |
100,00 |
100,00 |
|||
|
rstRElТor(VC1455) |
100,00 |
100,00 |
100,00 |
100,00 |
|||
|
Остров патогенности VPI-I |
aldA (VC0819) |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
|
mop (VC0823) |
100,00 |
100,00 |
100,00 |
100,00 |
97,7 |
97,7 |
|
|
tcpA (VC0828) |
99,85 |
99,85 |
100,00 |
100,00 |
80,4 |
80,4 |
|
|
toxT (VC0838) |
100,00 |
100,00 |
100,00 |
100,00 |
99,88 |
99,88 |
|
|
acfB (VC0840) |
100,00 |
100,00 |
100,00 |
100,00 |
99,89 |
99,89 |
|
|
Остров патогенности VPI-II |
100,00 |
100,00 |
100,00 |
100,00 |
99,90 |
99,90 |
|
|
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
||
|
nanH (VC1784) |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
|
|
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
||
|
Остров пандемичности VSP-I |
100,00 |
100,00 |
100,00 |
100,00 |
|||
|
100,00 |
100,00 |
100,00 |
100,00 |
||||
|
99,93 |
100,00 |
100,00 |
100,00 |
||||
|
100,00 |
100,00 |
100,00 |
100,00 |
||||
|
100,00 |
100,00 |
100,00 |
100,00 |
||||
|
Остров пандемичности VSP-II |
100,00 |
100,00 |
100,00 |
100,00 |
|||
|
100,00 |
100,00 |
||||||
|
type IV pilin (VC0502) |
100,00 |
100,00 |
|||||
|
Кластер RTX |
RTX toxin RtxA (VC1451) |
100,00 |
100,00 |
100,00 |
100,00 |
||
|
RTX toxin transporter (VC1447) |
100,00 |
100,00 |
100,00 |
100,00 |
99,86 |
99,93 |
|
|
Кластер MSHA |
mshA (VC0409) |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
|
proteinCsrD (VC0398) |
99,85 |
99,85 |
99,80 |
99,80 |
99,85 |
99,85 |
|
|
MSHA pilin protein MshD (VC0411) |
100,00 |
100,00 |
99,84 |
99,84 |
100,00 |
100,00 |
|
|
Система секреции шестого типа (T6SS) |
vasA (VCA0110) |
100,00 |
100,00 |
100,00 |
100,00 |
99,44 |
99,44 |
|
vasF (VCA0115) |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
|
|
vasK (VCA0120) |
100,00 |
100,00 |
100,00 |
100,00 |
99,87 |
99,87 |
|
|
vgrG3 (VCA0123) |
100,00 |
100,00 |
100,00 |
100,00 |
99,93 |
99,93 |
|
|
Tol-кластер и локус vps |
tolQ (VC1839) |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
|
TolA (VC1837) |
100,00 |
100,00 |
99,91 |
100,00 |
100,00 |
100,00 |
|
|
TolR (VC1838) |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
|
|
vpsA (VC0917) |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
|
|
vpsL (VC0934) |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
100,00 |
|
|
100,00 |
100,00 |
100,00 |
100,00 |
80,40 |
80,40 |
||
|
99,66 |
99,66 |
100,00 |
100,00 |
99,84 |
99,84 |
||
|
100,00 |
100,00 |
100,00 |
100,00 |
99,89 |
99,89 |
||
Как видно из таблицы, полногеномное секвенирование стрессированных культур не выявило полиморфизма структуры генома в сравнении с исходными штаммами по основным наборам генов.
В связи с тем, что в литературе есть сведения об изменениях VNTR-профиля холерных вибрионов на начальном этапе стрессового воздействия у отдельных штаммов, которые рассматриваются авторами как первичная реакция на стресс , вероятно, следует учитывать их при анализе результатов молекулярного типирования вибрионов, выделенных в рамках проведения мониторинга при эпидемиологическом надзоре за холерой. В связи с этим возникала необходимость выбора более стабильного метода типирования выделяемых штаммов холерных вибрионов, в том числе разработанного А.С. Водопьяновым INDEL-типирование . Проведение INDEL-типирования исследуемых штаммов по 9 локусам показало, что все изученные стрессированные культуры сохранили свой INDEL-профиль без изменений (табл. 2).
Таблица 2
Результаты INDEL-типирования исходных и стрессированных культур холерных вибрионов
|
№ п/п |
№ штамма |
Дата выде-ления |
Место выделения |
Источник выделения |
INDEL-аллель по локусам |
||||||||||
|
г.Таганрог |
морская вода |
+ |
+ |
||||||||||||
|
стрессир.1 |
+ |
+ |
|||||||||||||
|
стрессир.2 |
+ |
+ |
|||||||||||||
|
г. Таганрог |
больной |
+ |
+ |
||||||||||||
|
стрессир.1 |
+ |
+ |
|||||||||||||
|
стрессир.2 |
+ |
+ |
|||||||||||||
|
569В (классич.) |
Индия |
больной |
+ |
+ |
|||||||||||
|
569В -1 |
стрессир.1 |
+ |
+ |
||||||||||||
|
569В -2 |
стрессир.2 |
+ |
+ |
||||||||||||
Выводы. Таким образом, токсигенные холерные вибрионы могут персистировать в воде открытых водоемов при температуре 22°С-24°С достаточно продолжительный срок с сохранением продукции холерного токсина, т.е. оставаясь эпидемически значимыми; при понижении температуры до 10°С и ниже уровни токсинопродукции снижаются вплоть до отрицательных значений, а низкая температура как стрессор, имитирующий условия окружающей среды в речной воде в холодное время года, возможно, ингибирует активацию белка ToxT, ответственного за транскрипцию генов, кодирующий холерный токсин, уже в первый месяц. Установлено, что, вне зависимости от отрицательных показателей ИФА, гены ctхAB обнаруживаются в ПЦР до тех пор, пока в популяции исследуемых штаммов сохраняются живые вибрионы. В «пустых» пробах, исследуемых после гибели всей популяции V.cholerae, гены, ответственные за токсинопродукцию, не обнаруживаются. Изменений в популяции клеток вибрионов, выживших после низкотемпературного стресса, связанных с утратой профага CTXφ, несущего гены, ответственные за синтез холерного токсина, а также утратой других значимых участков генома, в наших экспериментах не отмечено, что подтверждается в полногеномном секвенировании INDEL-типировании исходных и стрессированных культур и говорит о его стабильности. Возможно, изменение токсинопродукции в стрессовых условиях связано не с реорганизацией генома, а с изменением экспрессии каскада регуляторных генов ToxR-S, ToxT, регуляция которых находится в непосредственной зависимости от состояния кворум сенсинга бактериальной культуры V.cholerae и управляется четырьмя малыми РНК, получившими название Qrr1-4 . Возможно, регуляторная система малых РНК позволяет V.cholerae сохранять гены патогенности в стрессовых условиях, что и является предметом наших дальнейших исследований.
Содержание
Библиографическая ссылка
Сизова Ю.В., Писанов Р.В., Водопьянов А.С., Черепахина И.Я., Бурлакова О.С. ФЕНОТИПИЧЕСКИЙ И ГЕНОТИПИЧЕСКИЙ АНАЛИЗ ТОКСИНОПРОДУКЦИИ ТИПИЧНЫХ И АТИПИЧНЫХ ШТАММОВ ХОЛЕРНЫХ ВИБРИОНОВ В СТРЕССОВЫХ УСЛОВИЯХ ОКРУЖАЮЩЕЙ СРЕДЫ // Современные проблемы науки и образования. – 2017. – № 3.;
URL: http://science-education.ru/ru/article/view?id=26439 (дата обращения: 27.11.2019). Предлагаем вашему вниманию журналы, издающиеся в издательстве «Академия Естествознания» (Высокий импакт-фактор РИНЦ, тематика журналов охватывает все научные направления) «Современные проблемы науки и образования» список ВАК ИФ РИНЦ = 0.791 «Фундаментальные исследования» список ВАК ИФ РИНЦ = 1.074 «Современные наукоемкие технологии» список ВАК ИФ РИНЦ = 0.909 «Успехи современного естествознания» список ВАК ИФ РИНЦ = 0.736 «Международный журнал прикладных и фундаментальных исследований» ИФ РИНЦ = 0.570 «Международный журнал экспериментального образования» ИФ РИНЦ = 0.431 «Научное Обозрение. Биологические Науки» ИФ РИНЦ = 0.303 «Научное Обозрение. Медицинские Науки» ИФ РИНЦ = 0.380 «Научное Обозрение. Экономические Науки» ИФ РИНЦ = 0.600 «Научное Обозрение. Педагогические Науки» ИФ РИНЦ = 0.308 «European journal of natural history» ИФ РИНЦ = 1.369 Издание научной и учебно-методической литературы ISBN РИНЦ DOI
Анализ фенотипической изменчивости
Цель:расширить и углубить знания о взаимосвязи генотипа и окружающей среды, сформировать умения описывать фенотип растений, сформировать знания о статистическом характере закономерностей модификационной изменчивости, о вариационном ряде изменчивости признака.
Вопросы входного контроля:
1. Какие общебиологические закономерности лежат в основе создания новых пород и сортов? Знания из каких областей наук необходимы селекционеру для успешной работы?
2. Какая связь между модификационной изменчивостью и генотипом любого организма? Приведите примеры.
3. Каким образом можно проверить наследуемость фенотипических признаков? Приведите примеры.
Общие сведения:Модификационная изменчивость — это результат не изменений генотипа, а его реакции на условия окружающей среды. При модификационной изменчивости наследственный материал не изменяется, — изменяется проявление генов.
Под действием определенных условий окружающей среды на организм изменяется течение ферментативных реакций (активность ферментов) и может происходить синтез специализированных ферментов, некоторые из которых ответственны за регуляцию транскрипции генов, зависящую от изменений окружающей среды. Таким образом, факторы окружающей среды способны регулировать экспрессию генов, то есть интенсивность выработки ими специфических белков, функции которых отвечают специфическим факторам окружающей среды.
Предел проявления модификационной изменчивости организма при неизменном генотипе — норма реакции. Норма реакции обусловлена генотипом и различается у разных особей данного вида. Фактически норма реакции — спектр возможных уровней экспрессии генов, из которого выбирается уровень экспрессии, наиболее подходящий для данных условий окружающей среды. Норма реакции имеет пределы или границы для каждого биологического вида (нижний и верхний) — например, усиленное кормление приведет к увеличению массы животного, однако она будет находиться в пределах нормы реакции, характерной для данного вида или породы. Норма реакции генетически детерминирована и наследуется. Для разных признаков пределы нормы реакции сильно различаются. Например, широкие пределы нормы реакции имеют величина удоя, продуктивность злаков и многие другие количественные признаки), узкие пределы — интенсивность окраски большинства животных и многие другие качественные признаки.
Тем не менее, для некоторых количественных признаков характерна узкая норма реакции (жирность молока, число пальцев на ногах у морских свинок), а для некоторых качественных признаков — широкая (например, сезонные изменения окраски у многих видов животных северных широт). Кроме того, граница между количественными и качественными признаками иногда весьма условна.
Оборудование:Экземпляры растений одного вида или сорта. Наборы биологических объектов: семена фасоли, бобов, колосья пшеницы, клубни картофеля, листья яблони, акации и пр. Линейка.
Порядок выполнения работы:
Фенотипы крови человек
Мы все или почти все, знаем или что-то слышали, о том, что совместимость крови при переливании определяется наличием или отсутствием следующих антигенов:
Групповые антигены системы АВ0: А и B — наиболее значимые.
Сочетание этих антигенов определяет группу крови 0(I), A(II), B(III) или AB(IV);
- группа А — на поверхности эритроцитов находится только антиген А,
- группа В — на поверхности эритроцитов находится только антиген В,
- группа АВ — на поверхности эритроцитов находятся антигены как А, так и В,
- группа 0 — на поверхности эритроцитов нет ни антигена А, ни антигена В.
Если у человека группа крови А, В или 0, то в его плазме крови имеются также и антитела, которые уничтожают те антигены, которых у самого человека нет. Примеры: Если у вас группа крови А, то вам нельзя переливать кровь группы В, ибо в таком случае в вашей крови имеются антитела, которые борются против антигенов В. Если у вас группа крови 0, то в вашей крови имеются антитела, которые борются как против антигенов А, так и против антигенов В.
Частота встречаемости групп крови: первая О (I) (составляет 33,5 % от общего населения планеты), вторая A (II) (37,8 %), третья B (III) (20,6 %), четвертая AB (IV) (8,1 %).
Антигены системы резус находятся на втором месте по значимости после системы АВ0.
Эта система насчитывает более 50 антигенов. Основные антигены системы резус: D, d, С, с, Е, е. Они образуют три пары антигенов: DD, dd, СС, сс, ЕЕ, ее, Dd, Cc, Ее. Частота встречаемости антигенов системы Резус: D — 85 %, С — 70 %, Е — 30 %, с — 80 %, е — 97 %. Наиболее частые фенотипы: CcDEe — 14 %, CcDee — 32 % , ccDEe — 12 % , CCDee — 19,5 % , ccDee — 3 % , ccddee — 13 % , Ccddee — 1,5 %.
Редким фенотипом крови считается фенотип, редко встречающийся в популяции. К примеру, фенотип ccddee — резус-отрицательный имеют около 13 % населения, а фенотип ссDEE — 3 %, (отсутствует антиген е). При необходимости переливания крови реципиенту, имеющему такой фенотип, это становится жизненно важно, так как на отсутствующие у реципиента антигены организм может вырабатывать антитела.
Наиболее активным является антиген D, который и подразумевается под термином «резус-фактор». Именно по наличию или отсутствию антигена D все люди делятся на резус-положительных и резус-отрицательных.
Антигены Kell
Частота встречаемости 7–9 %. В настоящее время насчитывается 24 антигена системы Kell , наибольшее клиническое значение имеет антиген К из-за высокой иммуногенности. У людей с нехваткой специфического антигена Kell могут вырабатываться антитела против антигенов Kell, когда делается переливание крови, содержащей этот антиген. При последующих переливаниях крови могут отмечаться разрушения новых клеток этими антителами — процесс, известный как гемолиз. Лицам, не имеющим антигенов Kell (K0), при необходимости эритроциты переливаются только от Kell-отрицательных доноров для предотвращения гемолиза. По этой причине от Кell-положительных доноров в общем случае заготавливаются только те препараты крови, в которых нет эритроцитов: плазма, тромбоконцентрат или криопреципитат. Лица же с отрицательным антигеном Kell являются универсальными по этому признаку реципиентами эритроцитов, так как не происходит их отторжения.