Содержание
Введение
Острые респираторные вирусные инфекции (ОРВИ) вызываются разнообразными возбудителями, среди которых вирусы парагриппа, аденовирусы, риновирусы, реовирусы и др. — всего более 300 вирусов. Это самая распространенная группа среди инфекционных заболеваний, характеризующаяся обычно непродолжительной лихорадкой, поражением респираторного тракта и интоксикационным синдромом. Показатели заболеваемости гриппом и ОРВИ ежегодно в России высокие — от 27,3 млн до 41,2 млн человек, заболеваемость гриппом в мире — до 1 млрд случаев, из которых от 3 млн до 5 млн — тяжелые формы. Случаи летальности от гриппа и его осложнений в мире составляют от 250 тыс. до 500 тыс. человек, при этом в последние десятилетия не было отмечено снижения показателей смертности от гриппозной пневмонии .
Профилактика инфекций дыхательных путей предусматривает использование специфических и неспецифических медицинских средств. Специфическая вакцинопрофилактика существует только для гриппа. Однако с учетом того, что удельный вес гриппа в структуре заболеваемости ОРВИ составляет не более 1%, применение только противогриппозных вакцин не позволяет решить проблему. Широкое распространение получил отечественный препарат умифеновир, который рекомендуется для лечения и профилактики гриппа и ОРВИ у взрослых и детей. Многочисленные экспериментальные и клинические исследования показали, что эффективность умифеновира обусловлена непосредственно вирус-специфическим действием. По механизму противовирусного действия он относится к ингибиторам слияния (фузии), взаимодействует с гемагглютинином вируса и препятствует слиянию липидной оболочки вируса и клеточных мембран. Оказывает умеренное иммуномодулирующее действие. Обладает интерферон-индуцирующей активностью, стимулирует гуморальные и клеточные реакции иммунитета, фагоцитарную функцию макрофагов, повышает устойчивость организма к вирусным инфекциям .
Значительные успехи в области иммунологии в последние десятилетия открыли перспективы для пересмотра прежних представлений о возможностях первичной профилактики ОРВИ и создания соответствующих лекарственных средств. Основными требованиями к разрабатываемым препаратам являлись губительное воздействие на большинство респираторных вирусов в сочетании с нормализацией состояния иммунной системы и повышением неспецифической резистентности организма к респираторной вирусной инфекции при отсутствии побочных эффектов.
Иммунитет слизистых реализуется через единую структурированную систему, получившую название «мукоза-ассоциированная лимфоидная ткань» (МАЛТ, mucosa-associated lymphoid tissue). МАЛТ — это самая большая часть иммунной системы, где на общей площади 400 м2 располагаются около 50% иммунокомпетентных клеток (клетки врожденного и приобретенного иммунитета) . МАЛТ обеспечивает многоуровневую защиту организма от проникновения патогенов и чужеродных веществ: от «пассивной» гуморальной защиты через активный антиген-неспецифический врожденный иммунитет к высокоспецифическому адаптивному иммунитету, с возможностью перехода с местного уровня на системный.
Помимо единой структурной организации существует еще одна особенность — активация адаптивного иммунитета в какой-либо части МАЛТ приводит к формированию пула антиген-специфических клеток, часть которого остается в месте начала иммунного ответа, а другая выходит в системный кровоток и расселяется (хоминг) в другие компартменты МАЛТ. За счет этого механизма формируется глобальная защита всех барьерных тканей .
Учитывая все возможные опосредованные механизмы воздействия на иммунную систему, представляется оптимальным использование при ОРВИ препаратов интерферона (ИФН). Интерфероны физиологичны, являются естественными медиаторами детально исследованных эффекторных и регуляторных сигналов иммунной системы. Топические формы ИФН вводятся непосредственно в первичные места проникновения вирусов в верхних отделах дыхательных путей и действуют на соответствующие рецепторы эпителиальных и других клеток этого биотопа, а для ректальных форм ИФН конечной мишенью являются нижние отделы респираторного тракта, куда они могут попасть через прямокишечные вены. Доказано, что топические и ректальные формы ИФН приемлемы для укрепления противоинфекционной защиты в разных отделах респираторного тракта .
Многие годы интерфероны успешно используются для лечения ОРВИ и гриппа, в частности, препарат Виферон® (ООО «Ферон», Россия). Имеющиеся научные данные характеризуют Виферон® как иммуномодулирующий препарат с выраженным противовирусным эффектом ,
он выпускается в виде ректальных свечей (регистрационный номер 000017/01), содержащих ИФН альфа-2b (ИФН α-2b) и высокоактивные антиоксиданты — витамины Е и С в 4 различных дозировках: 150 тыс. МЕ, 500 тыс. МЕ, 1 млн и 3 млн МЕ. Мы в своей работе использовали Виферон® в дозе 1 млн МЕ, альфа-токоферола ацетат (0,055 г) и аскорбиновую кислоту (0,0081 г). Также препарат выпускается в виде мази и геля для наружного и местного применения (регистрационный номер геля 001142/02, регистрационный номер мази 001142/01). Лекарственная форма в виде геля использовалась нами интраназально, что обеспечивает простой, безопасный и безболезненный способ применения препарата. Гель Виферон® — комплексный отечественный препарат , содержащий ИФН α-2b
(36 000 МЕ / 1 г), альфа-токоферола ацетат (0,055 г), бензойную кислоту (0,00128 г) и лимонной кислоты моногидрат (0,001 г). Природный антиоксидант витамин Е и его синергисты — лимонная и бензойная кислоты, метионин способствуют стабилизации клеточных мембран. Гелевая основа обеспечивает пролонгированное действие препарата, образует защитную пленку, предохраняющую от вторичного инфицирования.
Цель работы: оценка клинико-иммунологической эффективности комбинации ректальной и топической форм ИФН α-2b (Виферон®) в лечении ОРВИ у взрослых.
Материал и методы
В 2016–2018 гг. под наблюдением в условиях поликлиники № 180, НККДЦ ЦНИИ Эпидемиологии и ИГБ № 2 находились 89 пациентов (из них 48 мужчин и 41 женщина в возрасте от 18 до 45 лет, средний возраст — 28,3±1,9 года) с неосложненными формами ОРВИ на момент обращения. Все пациенты были включены в исследование не позднее 48 ч от момента появления первых симптомов заболевания.
Критерии исключения из исследования: пациенты, принимавшие противовирусные и иммуномодулирующие препараты в течение 1 мес. до заболевания,
а также имеющие в анамнезе хронические заболевания органов дыхания, сердечно-сосудистой и эндокринной систем; больные ОРВИ с осложнениями в момент скрининга; выявление респираторных инфекций Chlamydia pneumoniae и Mycoplasma pneumoniae; проявившаяся в ходе исследования аллергическая реакция на лекарственные препараты; несоблюдение кратности и схемы приема препарата; отказ пациента от продолжения участия в исследовании.
Также была обследована группа из 30 условно здоровых лиц (контрольная группа), сопоставимых по возрасту и полу с основной группой, не болевших респираторными инфекциями и не принимавших антибактериальные и противовирусные препараты в течение последних 6 мес.
Всем пациентам после подписанного информированного согласия на участие в исследовании проведено комплексное обследование, включавшее в себя клинический анализ крови, общий анализ мочи; верификацию возбудителей респираторной инфекции методом полимеразной цепной реакции (ПЦР) — исследование мазков из носа и ротоглотки на респираторные инфекции в лаборатории ЦНИИЭ. Исследования концентрации секреторного иммуноглобулина А (sIgA) в назальных пробах (экстракция мазка из носа в 1 мл физиологического раствора методом иммуноферментного анализа (ИФА) (тест-системы
АО «Вектор-БЕСТ», Россия) и уровней сывороточного ИФН, спонтанной и индуцированной концентрации цитокинов ИФН-α, ИФН-γ в сыворотке крови проводили на базе лаборатории онтогенеза и коррекции системы интерферона ФГБУ «НИЦЭМ им. Н.Ф. Гамалеи» Минздрава России. Концентрацию ИФН-α и ИФН-γ в плазме крови и супернатантах культур клеток крови определяли методом твердофазного «сэндвич»-варианта иммуноферментного анализа (ИФА) с помощью наборов АО «Вектор-Бест» на микропланшетном ридере Anthos 2020 (Австрия).
Больные были рандомизированы в 2 сопоставимые группы. В 1-й (основной) группе (n=46) пациенты в течение
5 дней в составе комплексного лечения получали 2 р./сут ректальные свечи Виферон®, содержащие 1 млн МЕ ИФН α-2b, и интраназально Виферон® гель для наружного и местного применения, содержащий 36 000 МЕ / 1 г ИФН α-2b, 3 р./сут в течение 5 дней. Во 2-й группе (сравнения) (n=43) больным назначали умифеновир по 200 мг 4 р./сут в течение 5 дней.
Помимо противовирусной терапии пациенты получали симптоматическое лечение (ирригационные процедуры, деконгестанты, парацетамол/ибупрофен при температуре выше 38,5 °C). Характеристика групп наблюдения представлена в таблице 1.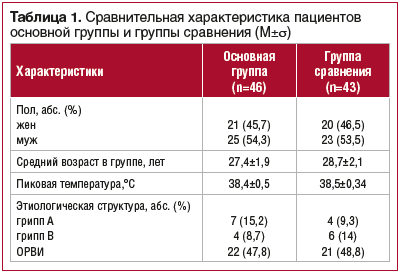
Все исследования проводились в динамике: в 1-й день включения и на следующий день после окончания терапии; по необходимости проводились пульсоксиметрия, рентгенография органов грудной клетки, электрокардиография.
В процессе лечения ежедневно регистрировались субъективные жалобы пациентов в дневнике самоконтроля состояния, проводилась термометрия 2 р./сут, осуществлялись осмотр и контроль ведения дневника пациентом в 1-й и 6-й дни терапии. Проводилась оценка эффективности противовирусной терапии по клинико-лабораторным данным в группах сравнения в динамике.
Математическую обработку данных осуществляли с помощью программы Statistica 8 (StatSoftInc). Сравнение независимых выборок по количественным характеристикам проводили с помощью критерия Манна — Уитни. Результаты сравнений считались статистически значимыми при р<0,05.
Результаты исследования
Клиническая картина заболевания была типичной, заболевание начиналось остро: с лихорадки, интоксикации, катарально-респираторного синдрома разной степени выраженности. Основными жалобами были повышение температуры, преимущественно сухой кашель, боль и першение в горле, насморк и/или заложенность носа, слабость, головная боль, ломота в теле. Методом ПЦР у пациентов были выявлены грипп типа А и В у 11 (12,4%) и 10 (11,2%) больных соответственно, риновирус (РВИ) — у 11 (12,4%), аденовирус (АДВИ) — у 15 (16,9%), РС-вирус — у 7 (7,9%), парагрипп — у 3 (3,4%), микст-инфекции (сочетание различных респираторных инфекций) — у 5 (5,6%). В 30,3% (n=27) случаев не удалось обнаружить возбудителей респираторных инфекций.
Клинические и лабораторные показатели во всех случаях свидетельствовали о легком или среднетяжелом течении заболевания. Клинико-лабораторная характеристика больных ОРВИ в зависимости от этиологии представлена в таблице 2. Грипп характеризуется выраженной интоксикацией, лейкопенией и длительно сохраняющейся астенизацией. АДВИ характеризуется лейкоцитозом, выраженным катаральным синдромом на фоне умеренно выраженной интоксикации и лимфоаденопатией в 68% случаев.
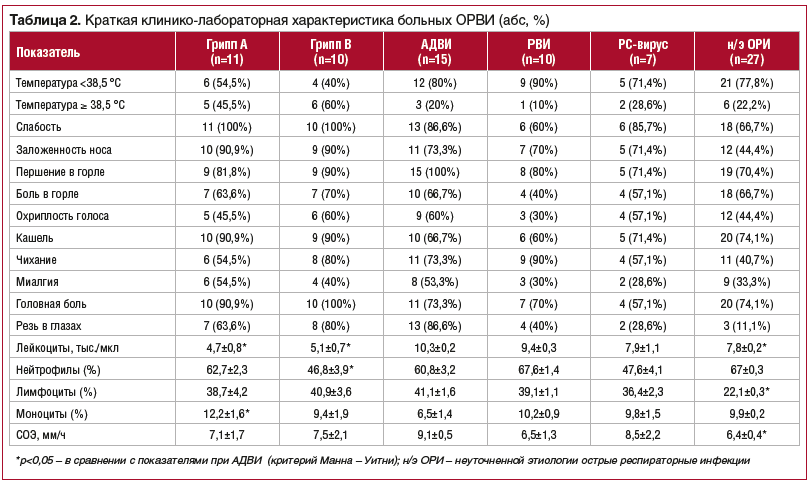
Анализ основных клинических симптомов в сравниваемых группах не выявил значимых различий в их частоте до начала терапии, что позволило объективно оценить клиническую эффективность различных схем терапии. Сравнительный анализ эффективности терапии оценивался по следующим критериям: сроки нормализации температуры, сроки исчезновения основных клинических симптомов, элиминация вируса после терапии. Сравнительный анализ продолжительности основных клинических синдромов в группах наблюдения представлен в таблице 3.
В проведенном сравнительном исследовании клинической эффективности противовирусной терапии ОРВИ в обеих группах получены сопоставимые результаты, однако прослеживается выраженная тенденция к сокращению продолжительности лихорадочного периода, интоксикационного синдрома и астенизации в основной группе. На 3-й день (по дневнику контроля) значительное улучшение наблюдалось в обеих группах, но в основной группе улучшение отмечалось в 76,7% случаев, тогда как в группе сравнения — в 65,7% случаев. На 5-й день терапии в основной группе у 1 больного (2,2%) не было улучшения
(с 3-го дня), выявлен острый бронхит, назначена соответствующая терапия. В группе сравнения у 3 больных (7%) отсутствовало улучшение с 3-го дня, 2 пациентам назначена антибактериальная терапия (синусит, тонзиллит). Отмечается меньшая динамика в элиминации АДВИ на 6-й день лечения: 49% — в основной группе и 41% — в группе сравнения при клинической стабилизации и на фоне выраженной положительной динамики в 97% случаев в основной группе и в 93% случаев в группе сравнения.
При оценке интерферонового статуса выявлены низкая концентрация ИФН-α в сыворотке крови и отсутствие спонтанной продукции в 74% случаев. Индуцированная выработка ИФН-α клетками крови у больных ОРВИ снижена, и сравнительный анализ не выявил межгрупповых отличий по этому показателю до лечения. Наблюдалось более значимое повышение уровня ИФН-α в основной группе при снижении уровня индуцированной продукции ИФН-α в сыворотке крови больных в группе сравнения после терапии. У больных оказались исходно статистически значимо ниже показатели индуцированной продукции ИФН-γ, чем у здоровых лиц (p<0,05). Выявлено повышение индуцированной продукции ИФН-γ в группе сравнения, в то время как применение комбинации ректальной и топической формы Виферона не оказывало значимого влияния на продукцию ИФН-γ (рис. 1).
Оценка продукции секреторного иммуноглобулина А (sIgA) в назальных пробах не выявила значимых отклонений между группами наблюдения. После лечения (рис. 2) выявлены достоверное повышение продукции sIgA (1,32±0,12 мг/л) в основной группе и выраженное снижение его продукции в группе сравнения — до 0,84±0,11 мг/л. Такой эффект ИФН объясняется усилением секреции sIgA эпителиоцитами и значительным влиянием на гуморальный иммунитет, что обеспечивает выраженный протективный эффект при проведении профилактики инфицирования патогенами.
В период наблюдения не отмечено никаких нежелательных явлений при применении препаратов умифеновир и Виферон® в ректальной и интраназальной формах. Лекарственные средства хорошо переносились, не вызывали аллергических реакций и побочных эффектов.
Заключение
Результаты исследования свидетельствуют, что совместное применение ректальных и топических форм ИФН α-2b (Виферон® свечи + Виферон® гель) позволяет получать положительные результаты, которые можно видеть при оценке клинической эффективности лечения: сокращается продолжительность лихорадочного периода, интоксикационного синдрома и астенизации, снижается число бактериальных осложнений, ускоряется достижение клинической ремиссии. Положительные клинические эффекты, как правило, сопровождаются позитивной динамикой со стороны показателей иммунной системы. Комбинация ректальной и топической форм ИФН α-2b (Виферон® свечи + Виферон® гель) обеспечивает положительную клиническую динамику к 3-му дню от начала лечения, является эффективной и безопасной терапией для больных ОРВИ и гриппом (97%). Кроме того, по эффективности эта комбинация сопоставима с терапией умифеновиром (93%) и даже превосходит его по иммуномодулирующему и протективному эффекту.
Исходя из полученных данных доказано, что совместное применение препарата Виферон® в форме суппозиториев и геля в комплексной терапии ОРВИ и гриппа решает вопрос выбора эффективного и безопасного средства.
Читать в полной версии Фото: Андрей Гордеев / Ведомости / ТАСС
Министерство здравоохранения расширило список препаратов, возможных к назначению для лечения COVID-19 у взрослых. Об этом свидетельствуют обновленные методические указания Минздрава по COVID-19.
В списке возможных к назначению взрослым лекарств упоминаются гидроксихлорохин, лопинавир + ритонавир, хлорохин, интерфероны (рекомбинантный интерферон бета-1b и рекомбинантный интерферон альфа), азитромицин (в комбинации с гидроксихлорохином). Ранее Минздрав уже рекомендовал эти препараты для лечения больных с коронавирусом. В списке также упоминается мефлохин и умифеновир.
В документе также говорится, что для упреждающей противовоспалительной терапии COVID-19 у взрослых можно использовать дексаметазон, препарат против артрита тоцилизумаб, барицитиниб и сарилумаб, антивоспалительное средство метилпреднизолон.
Среди всех лекарств наиболее перспективным в новых рекомендациях Минздрава называют противомалярийные средства хлорохин, гидроксихлорохин и мефлохин. По имеющимся данным, они препятствуют проникновению вируса в клетку и его репликации. Гидроксихлорохин в комбинации с азитромицином приводит к усилению лечебного эффекта.
Полная версия материала доступна только на сайте
В середине апреля глава Минздрава Михаил Мурашко сообщил, что в России разработали лекарство против коронавируса. Препарат уже испытали в нескольких странах. Доклинические испытания его проведены, их результаты оценивают специалисты.
До этого ученые из Японии объявили, что антиретровирусный препарат нелфинавир блокирует размножение вируса, вызывающего COVID-19. Японцы изучили девять препаратов, используемых против ВИЧ, и пришли к выводу, что нелфинавир останавливает репликацию коронавируса даже при приеме в малых дозах.
Полная версия материала доступна только на сайте
Так началась «эра интерферона». Человечество обрело мощное естественное средство для борьбы с вирусными инфекциями. Сегодня интерфероны — это большой класс белковых веществ, объединенных общим названием и имеющих сходные свойства. Наиболее изученным свойством данной группы белков является их способность препятствовать размножению вирусов, а также активизировать иммунную систему. В настоящее время в качестве лекарственных средств широко применяются интерфероны первого типа — альфа и бета. Рекомбинантные ИФН сегодня по праву считаются наиболее перспективными. Полученные методами генной инженерии без использования крови человека, эти ИФН отличаются чистым и однородным составом, высоким профилем безопасности и относительно низкой себестоимостью.
В записную книжку
Для лечения и экстренной профилактики гриппа и ОРВИ врачи рекомендуют оригинальный отечественный препарат Гриппферон®.
Состав: активный компонент — интерферон альфа-2b человеческий рекомбинантный не менее 10 000 ME, полимерная основа.
Показания к применению: Профилактика и лечение гриппа и ОРВИ у детей с рождения и взрослых.
Гриппферон®:
- выпускается в двух удобных лекарственных формах — капли назальные и спрей назальный дозированный;
- препарат топического действия, т.е. оказывает прямое противовирусное воздействие непосредственно в месте проникновения вируса в организм человека — в слизистой оболочке носовой полости;
- блокирует механизм воспроизведения респираторных вирусов;
- вирусы не способны приобрести устойчивость к действию препарата;
- разрешен пациентам всех категорий, в т.ч. детям с рождения, беременным и кормящим женщинам;
- на 60—70% снижает количество осложнений у больных с острой респираторной инфекцией;
- совместим с другими противовирусными препаратами, а также с вакцинопрофилактикой;
- не требует совместного назначения сосудосуживающих средств, так как сам уменьшает отек слизистой оболочки носа.

Способ применения и дозы:
При первых признаках заболевания Гриппферон® применяют в течение 5 дней в возрастной дозировке, по 1—3 капли/дозы в каждый носовой ход, от 3 до 5—6 раз в день (в соответствии с возрастом заболевшего). Так, у самых маленьких пациентов (в возрасте от 0 до 1 года) препарат применяют по схеме: 1 капля/доза Гриппферона в каждый носовой ход 5 раз в день (разовая доза — 1000 ME, суточная доза — 5000 ME). Взрослым (старше 14 лет) рекомендуется применять препарат по 3 капли/дозы 5—6 раз в день (разовая доза — 3000 ME, суточная доза — 15 000—18 000 ME).
Для профилактики Гриппферон® закапывают в разовой возрастной дозировке 2 раза в день на протяжении контакта с больным. При необходимости профилактические курсы повторяют.
Гриппферон® с лоратадином, мазь назальная — оригинальный безрецептурный комбинированный препарат, содержащий в своем составе рекомбинантный человеческий интерферон альфа-2b и антигистаминную субстанцию второго поколения — лоратадин. Препарат предназначен для лечения и профилактики гриппа и ОРВИ у взрослых, включая пациентов с аллергическим ринитом.
Как рекомендовать
Клиент: Здравствуйте! Похоже, я простудился. А у меня дочка маленькая и жена на четвертом месяце, болеть им совсем нельзя. Что лучше взять, чтобы и себе помочь, и близких защитить?
Первостольник: Возьмите Гриппферон® — он подходит и для лечения, и для профилактики гриппа и ОРВИ для всех членов семьи. Гриппферон® действует на причину заболевания — подавляет распространение вирусов в слизистой оболочке носа, помогает быстро снять основные симптомы болезни и снизить риск осложнений гриппа и ОРВИ¹.
Клиент: А беременным Гриппферон® можно?
Первостольник: Да, в течение всего срока. Препарат успешно прошел клинические испытания² и подтвердил свою безопасность, в т.ч. у беременных и у детей с рождения. А если болезнь протекает в легкой или средней форме, прием Гриппферона поможет избежать назначения антибиотиков — сами понимаете, как это важно для беременных.
Клиент: Хорошо, что безопасен для детей. А то у нас дочка часто болеет… Кстати, это таблетки? Мы ребенка никак не можем к таблеткам приучить.
Первостольник: Тогда точно Гриппферон® — то, что вам нужно! Это спрей или капли назальные. Такая форма помогает препарату сразу же начать работать на слизистой носа —именно там, где вирусы и проникают в организм.
Клиент: Хорошо, а как часто необходимо его закапывать?
Первостольник: Взрослому для лечения — по 3 капли/дозы спрея в каждую ноздрю 5—6 раз в сутки, 5 дней. Для профилактики Гриппферон® достаточно использовать всего дважды в сутки в возрастной дозе. Если же заболевание сопровождается аллергическими проявлениями, могу еще посоветовать мазь назальную Гриппферон® с лоратадином для взрослых. Препарат поможет избавиться от насморка, чиханья и других аллергических симптомов.
Клиент: Спасибо. Я возьму Гриппферон® для жены и дочки, а себе — Гриппферон® с лоратадином.
1Краснов В.В. Эффективность рекомбинантного интерферона альфа в лечении и профилактике ОРВИ. Вопросы практической педиатрии, 2016, т. 11, №4. — С. 44–52.
2Клинические и экспериментальные исследования Гриппферона проведены на 4450 испытуемых в 14 научно-исследовательских и клинических центрах России и Украины.
Опубликовано в журнале:
«Практика педиатра» № 1, 2019 (февраль) , стр. 3-6
Резюме: актуальность проблемы респираторных вирусных заболеваний обусловлена их чрезвычайно широким распространением, зачастую тяжелым течением, возможностью развития жизнеугрожающих осложнений и высоким экономическим ущербом, наносимым обществу в целом. В статье в сравнительном аспекте рассматриваются различные лекарственные средства, используемые в комплексной терапии острых респираторных вирусных инфекций у детей.
Ключевые слова: респираторные инфекции, индукторы интерферона, иммуномодуляция, дети, Циклоферон®
Abstract: the urgency of the problem of respiratory viral diseases is due to their extremely high spread, often severe, the possibility of developing life-threatening complications and the high economic damage caused to society as a whole. The article in a comparative aspect discusses the various drugs, used for the prevention and treatment of acute respiratory viral infections in children.
Keywords: respiratory infections, interferon inductors, immunomodulation, children, Cycloferon®
Острые респираторные вирусные инфекции (ОРВИ) остаются актуальной проблемой медицины в связи с их широким распространением и значительным экономическим ущербом, наносимым обществу. По статистике, экономические потери для России только в период эпидемии гриппа превышают 50 млрд руб. Также проблема остается серьезной в связи с частыми, порой жизнеугрожающими, осложнениями, возникающими на фоне или после перенесенного респираторного заболевания. Ежегодно заболеваемость детского населения ОРВИ превышает суммарную заболеваемость всеми остальными инфекциями . Заболеваемость у детей почти в 3 раза выше, чем у взрослых, а сама инфекция протекает тяжелее, элиминация вирусов из организма задерживается до 14 дней (у взрослых 4-6 дней). Причинами являются высокая контагиозность вирусов данной группы, наличие различных путей передачи, относительная устойчивость во внешней среде, скученность и длительное пребывание детей в закрытых помещениях в холодное время года и нестойкость иммунитета после перенесенного заболевания. Иммунная система у детей, особенно раннего возраста, обладает слабой противовирусной активностью, обусловленной низкой способностью лейкоцитов и лимфоцитов к продукции «ранних» ИНФ, их сниженными антивирусными и иммуномодулирующими свойствами. Считается, что у детей раннего возраста действие ИНФ направлено в большей степени на регуляцию развития, чем на антиинфекционную защиту. Кроме того, часто отмечается вторичное снижение иммунной реактивности организма ребенка на фоне течения ОРВИ, приводящее к слабому ответу на внедрение вируса в организм и обуславливающее затяжное и/или осложненное течение инфекции . Нельзя не упомянуть также о высокой скорости мутации вирусов и быстром формировании резистентности к противовирусным препаратам, что делает терапию противовирусными препаратами неэффективной.
Этиологическими факторами данной группы заболеваний являются около 300 эпителиотропных вирусов, из которых наиболее часто встречающимися у детей являются риновирусы, парагрипп, аденовирусы, грипп. В последние годы нарастает удельный вес таких возбудителей, как корона-, бока- и метапневмовирусы. Также ежегодно увеличивается доля различных микст-инфекций, вызывающих более тяжелое по течению респираторное заболевание, что существенно усложняет диагностику и лечение таких пациентов.
Клинические симптомы респираторных вирусных инфекций у детей во многом похожи и проявляются различной по степени тяжести и длительности лихорадкой, интоксикацией, катаральным синдромом и поражением дыхательных путей (табл. 1).
Таблица 1. Тропизм различных вирусов, вызывающих ОРВИ
| Вирус | Наиболее часто поражаемый орган |
| Гриппа | Трахея, носоглотка, сосуды |
| Парагриппа | Гортань |
| Аденовирус | Глотка, конъюнктива, кишечник |
| Риновирус | Полость носа |
| Реовирус | Носоглотка, кишечник |
| Коронавирус | Носоглотка, бронхи, кишечник |
| РС-вирус | Бронхиолы, альвеолы |
| Бокавирус | Носоглотка, кишечник |
| Метапневмовирус | Носоглотка, трахея, бронхи |
При гриппе на первый план выходит выраженный интоксикационный синдром и лихорадка, аденовирусная инфекция характеризуется болью в горле, конъюнктивитом, продуктивным кашлем, нередко — развитием обструктивного синдрома и болями в животе; при парагриппе часты ларингиты с развитием стеноза гортани, а при респираторно-синцитиальной инфекции -бронхит и/или бронхиолит с выраженным и длительным обструктивным синдромом. Однако различия симптоматики в зависимости от этиологии вирусного заболевания не всегда четко различимы, следовательно, практикующему врачу важно иметь в своем арсенале средства, одинаково эффективные для профилактики и лечения как гриппа, так и других ОРВИ.
Выбор метода лечения ОРВИ у детей зависит от возраста ребенка, клинической картины заболевания, выраженности симптомов, степени тяжести и наличия осложнений. Лечение обязательно должно включать режим, диету, медикаментозную и немедикаментозную терапию. Лекарственная терапия респираторных заболеваний у детей ориентирована на использование всего арсенала современных препаратов, отвечающих определенным критериям :
- высокая эффективность относительно большинства возбудителей;
- минимальный спектр побочных эффектов;
- отсутствие токсичности;
- сочетание противовирусного и иммуномодулирующего эффекта;
- наличие различных лекарственных форм;
По характеру воздействия лекарственные препараты, применяемые для лечения ОРВИ у детей, могут быть разделены на:
- этиотропные, действующие на возбудителя заболевания;
- патогенетические (иммуномодулирующие), исправляющие нарушения системы иммунитета, возникающие и развивающиеся в процессе болезни;
- симптоматические, предназначенные для купирования отдельных симптомов заболевания.
Препараты этиотропного действия, избирательно подавляющие различные звенья репродукции вирусов без негативного влияния на клетки макроорганизма, наиболее предпочтительны, однако, имеют ряд ограничений к использованию в педиатрической практике (табл. 2).
Таблица 2. Механизм действия различных противовирусных препаратов, применяемых при ОРВИ
| Действие | Механизм действия | Препарат |
| Ингибиторы нейраминидазы | Конкурентно и избирательно ингибирует нейроминидазу, что нарушает проникновение вируса в здоровые клетки, тормозит выход вирионов из инфицированной клетки | Осельтамивир, занамивир |
| Блокатор М-йонного канала (адамантаны) | Блокирует специфические ионные М-2 каналы, что приводит к нарушению процесса дезинтеграции вириона и высвобождению рибонуклеопротеида | Ремантадин, орвирем |
| Блокатор слияния, индуктор ИФН | Ингибирует слияние липидной вирусной оболочки с клеточной мембраной | Арбидол |
| Ингибитор РНК и ДНК вирусов | Конкурентное подавление образования гуанозин трифосфата, приводящее к нарушению синтеза вирусных РНК и ДНК | Рибавирин |
Так, ингибиторы нейраминидазы обладают избирательной активностью только против вирусов гриппа типа А и В, эффективны при назначении не позднее 48 ч от начала клинических симптомов заболевания, оказывают раздражающее действие на слизистую оболочку респираторного и пищеварительного тракта, вызывают тяжелые аллергические реакции вплоть до развития токсического эпидермального некролиза, а также имеют высокую стоимость. Препараты из группы адамантинов также обладают избирательной активностью против вируса гриппа А, вызывают побочные эффекты со стороны желудочно-кишечного тракта в виде тошноты и рвоты, нервной системы, проявляющиеся галлюцинациями и психозом, аллергическими реакциями. Кроме того, все противовирусные препараты эффективны только при раннем их применении, не позже 24-48 ч и приводят к возникновению штаммов вирусов с низкой чувствительностью или резистентностью к терапии. Лекарственная устойчивость является результатом мутаций вирусов и развивается, как правило, при многократном использовании препарата .
Основными патогенетически действующими группами препаратов являются интерфероны и их индукторы. Интерфероны — это группа биологически активных белков или гликопротеидов, синтезируемых клеткой в процессе защитной реакции на чужеродные агенты (экзогенные и/или эндогенные). Образование и действие интерферона составляет важнейший механизм врожденного (естественного) иммунитета. Доказано, что течение и исход вирусных инфекций во многом зависит от способности системы интерферона быстро реагировать на внедрение возбудителя . Всего в настоящее время описано более 100 различных эффектов интерферонов, основными из которых являются:
- подавление роста внутри- и внеклеточных инфекционных агентов вирусной и невирусной (хламидии, простейшие, бактерии) природы;
- антипролиферативная активность;
- антитуморогенный эффект;
- антимутагенный эффект;
- антитоксическое действие;
- радиопротективный эффект;
- иммуномодулирующий эффект(подавление или усиление продукции антител, стимуляция макрофагов, усиление фагоцитоза и др.).
Однако большое количество различных побочных эффектов, возникающих при использовании интерферонов, ограничивает их использование в педиатрической практике (рис. 1).
Рис. 1. Побочные эффекты препаратов интерферонового ряда 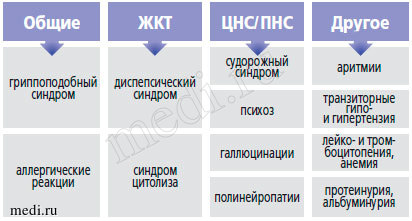
Лишены всех негативных эффектов интерферона препараты, относящиеся к группе его индукторов . Индукторы интерферона представляют собой группу низко- и высокомолекулярных природных и синтетических соединений, которые «включают» систему эндогенного интерферона. В настоящее время известны природные и синтетические соединения, которые в разной степени способны индуцировать активность интерферона (табл. 3) .
Таблица 3. Классификация индукторов интерферона (Ершов Ф.И., Романцов М.Г., Петров А.Ю., 2008)
| Химическая природа | Препарат |
| А. Синтетические соединения с основной интерферон-индуктивной активностью | |
| Низкомолекулярные: Флуореноны Акриданоны Олигопептиды Производное имидазо (4,5-С) квинолина |
Амиксин Циклоферон® аллокин-альфа имиквимод |
| Полимеры (дс-РНК) | Полудан, полигуацил |
| Б. Природные соединения с основной интерферон-индуктивной активностью | |
| Полифенолы | Кагоцел, мегосин, саврац рагосин, гозалидон |
| Полимеры (дс-РНК) | Ридостин, ларифан |
| Производные флавонидов и аминокислот | протефлазид |
| В. Иммунотропные препараты с вторичной интерферон-индуктивной активностью | |
| Т-миметики | Тимоген, тактивин, изопринозин, гроприносин, иммунофан |
| Иммуномодуляторы бактериального происхождения — эубиотики | Лактобактерин, биоспорин |
| Вакциноподобные препараты | Бронхомунал, рибомунил, ИРС-19, уроваксом |
| Липополисахариды | Пирогенал, продигиозан |
| Производные нуклеиновых кислот | Натрия нуклеинат |
| Препараты пурина и пиримидина | Метилурацил, пентоксил |
| Производные бензимидазола | Дибазол |
| Производные индола | Арбидол |
| Растительные иммунокорректоры | Родиола розовая, экстракт эхинацеи |
| Г. Препараты других фармакологических групп с вторичной интерферон-индуктивной активностью | |
| Метилксантины | Теофиллин, эуфиллин, дипиридамол, кофеин |
| Производные изохинолина | Папаверин, дротавирин |
| Производные бензофурана | Кордарон |
| Производные хромена | Интеркордин |
Немаловажным является то, что образование эндогенного интерферона при введении его индукторов является более физиологичным процессом, чем повторное введение экзогенных интерферонов, которые, помимо побочных эффектов, быстро выводятся из организма и угнетают образование собственных (аутологичных) интерферонов по принципу отрицательной обратной связи, что может привести к формированию хронического инфекционного процесса в организме ребенка . Имея основные свойства интерферона, его индукторы не обладают антигенностью и даже при однократном введении обеспечивают длительную циркуляцию синтезированных цитокинов на терапевтическом уровне. Стимулированный ими синтез эндогенного интерферона находится под контролем интерлейкинов и белков-репрессоров и не вызывает гиперинтерферонемии и развития связанных с ней побочных эффектов. Проведенные исследования показали, что индукторы интерферона обладают универсально широким диапазоном фармакологической активности, обладая одновременно прямым противовирусным и иммуномодулирующим действием. Введенные в организм индукторы интерферона стимулируют выработку эндогенного интерферона трех типов (α,β,γ) в разных пропорциях, что зависит от химической структуры индуктора. В зависимости от времени продукции интерферона в крови различают индукторы ранние (4-8 ч) и поздние (18-24 ч) .
Среди индукторов интерферона в профилактике и лечении ОРВИ у детей широко применяется препарат Циклоферон®, являющийся синтетическим производным акридонуксусной кислоты. Препарат повышает уровень интерферона α/β-типа в органах и тканях, содержащих лимфоидные элементы: в слизистой тонкого кишечника, селезенке, печени, легких, активирует стволовые клетки костного мозга, стимулируя образование гранулоцитов, преодолевает гематоэнцефалический барьер. Циклоферон® обладает чрезвычайно широким спектром биологической активности: прямым противовирусным, иммуномодулирующим и противовоспалительным действиями. Прямая противовирусная активность Циклоферона® доказана относительно различных респираторных вирусов и гриппа А и В, вируса простого герпеса 1-го и 2-го типов, цитомегаловируса, гепатитов В и С, клещевого энцефалита, вируса папилломы человека. Препарат нарушает репликацию вирусов, блокирует инкорпорацию вирусных ДНК и РНК в капсиды, что приводит к увеличению количества дефектных вирусных частиц и снижает вирус-индуцированный синтез белка в клетках. Иммунотропное действие препарата реализуется путем активации фагоцитов, Т-лимфоцитов и NK-клеток, нормализации баланса между CD4+- и СБ8+-клетками, снижении уровня В-лимфоцитов в периферической крови, с одновременным повышением синтеза высокоаффинных антител и индукции синтеза мРНК для ИФН-γ. Противовоспалительное действие Циклоферона® обусловлено ингибированием основных провоспалительных цитокинов (IL-1-p, IL-8, IL-10 и TNF-ot).
Циклоферон® относится к ранним индукторам интерферона, так как пик его выработки приходится на период от 4 до 8 ч с момента приема, что позволяет рекомендовать препарат для купирования вирусного заболевания на ранней стадии или в качестве экстренной профилактики. Кроме того, Циклоферон® хорошо сочетается с симптоматическими препаратами, вакцинами, химиопрепаратами, препаратами интерферона, усиливая действие последних и уменьшая побочные эффекты от их применения, что позволяет получить оптимальный фармакотерапевтический эффект. Исследование эффективности применения Циклоферона® в комплексном лечении ОРВИ у детей, проведенное Е.И. Кондратьевой, выявило более быстрое купирование симптомов интоксикации и выраженности катаральных явлений, обусловленное противовоспалительным и цитопротективным действием на слизистую оболочку дыхательных путей, а также увеличением уровня секреторного IgA. М.В. Гаращенко в своем исследовании отмечает почти 10-кратное уменьшение числа заболевших ОРВИ в период эпидемического подъема заболеваемости на фоне применения Циклоферона® (6 и 58% соответственно), а также более легкое течение и отсутствие осложнений .
Помимо высокой эффективности, препарат отличается высоким профилем безопасности, который подтверждается отсутствием токсичности, аллергенности, мутагенности, хорошей растворимостью в биологических средах и проникновением в ткани, быстрым выведением из организма и отсутствием кумуляции .
Таким образом, широкий спектр биологической активности при низкой токсичности, наличие иммуномодулирующего действия позволяют рекомендовать Циклоферон® как препарат первой линии в лечении острых респираторных инфекций у детей. Для наибольшей эффективности рекомендуется начинать применять Циклоферон® как можно раньше, дополняя его препаратами направленного этиотропного действия и иммуномодуляторами, что обеспечит достижение оптимального фармакотерапевтического эффекта.
ЛИТЕРАТУРА
Противовирусные белки интерфероны помогают организму быстрее избавиться от коронавируса, сообщают китайские ученые. Также интерфероны способствуют снижению воспаления в организме. Исследователи надеются, что их использование поможет эффективнее бороться с болезнью и сдерживать пандемию.
Использование интерферона способствует более быстрому излечению от COVID-19, полагают китайские ученые из Хуачжунского университета науки и технологии, а также их канадские и австралийские коллеги. Исследование было опубликовано в журнале Frontiers in Immunology.
Интерфероны — это белки, которые клетки организма выделяют в ответ на появление вирусов, некоторых бактериальных веществ и низкомолекулярных соединений. Они активируют определенные клеточные белки, которые не дают вирусу размножаться. Интерфероны в инъекционной форме используются при лечении вирусных гепатитов, рассеянного склероза и рака.
В виде таблеток, свечей, мазей и т. п. интерфероны бесполезны — в такой форме практически невозможно достичь в организме концентраций, которые позволили бы бороться с инфекцией.
«Интерфероны — это наша первая линия защиты от любых вирусов, но коронавирусы эволюционировали и научились блокировать эту реакцию, — говорит ведущий автор доктор Элеанор Фиш. — Однако лечение интерфероном отменяет ингибирующее действие вируса».
Исследователи предположили, что интерфероны могут быть эффективны, изучив их применение во время вспышки атипичной пневмонии 2002-2003 годов. В то время у пациентов, получавших интерфероны, болезнь проходила быстрее, чем у тех, кого лечили иными методами.
В этот раз авторы отобрали 77 пациентов с COVID-19 в одной из китайских больниц. Болезнь протекала в умеренной форме, никто из пациентов не нуждался в интенсивной терапии или ИВЛ.
Исследователи разделили пациентов на три группы. Одна в качестве лечения получала интерферон альфа-2b (синтетический интерферон, показавший эффективность при лечении ряда заболеваний) в концентрации 5 млн МЕ/мл ингаляционным методом, другая — арбидол (препарат с недоказанной эффективностью, заявленный как противовирусный), третья — и то, и другое.
Как оказалось, применение интерферонов ускоряло выведение вируса из организма в среднем на неделю.
Также в крови снижались уровни маркеров воспаления — С-реактивного белка и интерлейкина-6.
Несмотря на небольшую выборку, удалось продемонстрировать эффективность интерферона при лечении COVID-19, отмечают исследователи. Он способствует более быстрому выведению вируса из верхних дыхательных путей и уменьшению воспалительных процессов в организме.
«Вместо того, чтобы разрабатывать противовирусный препарат для каждого нового вируса, я бы предложила рассматривать интерфероны в качестве препаратов первой линии,
— говорит Фиш. — Интерфероны были одобрены для клинического использования в течение многих лет, поэтому можно попробовать «перепрофилировать» их на тяжелые, острые вирусные инфекции».
Пока что это первая работа, которая говорит об эффективности интерферона в борьбе с COVID-19. Исследователи говорят о необходимости двойного слепого плацебо-контролируемого исследования на более крупной выборке, чтобы уточнить данные. Также важно выяснить, какие результаты использование интерферона дает при лечении тяжелых случаев заболевания и как на результаты влияет наличие тех или иных хронических заболеваний. Если интерферон хорошо покажет себя и в дальнейших испытаниях, то его можно будет использовать в клинической практике, тем самым сокращая время лечения и замедляя распространение пандемии. Авторы работы отмечают важность поиска альтернатив, пока нет ни вакцины, ни эффективных противовирусных препаратов.
Ранее американские врачи также сообщили, что антикоагулянты позволяют в два раза снизить смертность от COVID-19.
Среди пациентов, получавших разжижающие кровь препараты, умерло в два раза меньше людей, чем среди тех, кто не их не получал.
При этом, однако, у получавших антикоагулянты пациентов чаще встречались кровотечения разных видов, от внутримозгового до желудочного, кровоизлияния в глаза и кровь в моче — таковых было 3%. В группе, не получавшей антикоагулянты, кровотечения и кровоизлияния наблюдались у 1,9%.
Коронавирусная инфекция повышает тромбообразование, поясняют ученые — от инсультов на фоне COVID-19 страдают даже молодые люди. Применение антикоагулянтов способно снизить риски закупорки сосудов. Однако для начала полученные данные предстоит перепроверить на большей когорте.




