Содержание
Почему так происходит и как этого избежать?
Причины этого явления еще недостаточно изучены, и хотя почти в каждом протоколе бывают случаи, что не оплодотворилась яйцеклетка при ЭКО, часть оплодотворенных яйцеклеток обычно составляет 70%. Это считается хорошим показателем, но он может быть различным в разных клиниках, когда зависит от методики проведения, питательной среды или опыта эмбриолога.
Но даже в самых благоприятных условиях, у опытного эмбриолога бывает, что при ЭКО не оплодотворились яйцеклетки, или из 15—16 развивающихся фолликулов только 1—2 ооцита оплодотворяются. Даже такие ооциты могут оказаться некачественными и не имплантироваться при переносе. Чтобы понять, почему не оплодотворяется яйцеклетка при ЭКО, нужно поэтапно изучить процедуру созревания и извлечения ооцитов.
Для получения яйцеклеток женщине проводят контролируемую стимуляцию яичников. В зависимости от диагноза, гормонального фона используют короткий или длинный протокол, для их проведения применяют различные гормональные препараты. Организм каждой женщины может по-разному отреагировать на тот или иной препарат. Так, неправильно подобранное лекарственное средство, дозировка, могут привести к тому, что во время стимуляции разовьется мало фолликулов, или, наоборот, возникнет синдром гиперстимулированных яичников.
За созреванием фолликулов наблюдают по УЗИ, и когда они достигают размера 18—20 мм, проводится пункция. Во время пункции не из всех фолликулов получают созревшие яйцеклетки. Некоторые из фолликулов не имеют яйценосного бугорка, с возрастом в яичниках женщины количество таких фолликулов увеличивается, поэтому количество фолликулов на УЗИ не всегда соответствует количеству полученных яйцеклеток.
Почему яйцеклетка не оплодотворяется. Гипотезы
Качество ооцитов также бывает различным. Фолликулы созревают неравномерно, и судить о том зрелая, недозрелая или перезрелая яйцеклетка находится в фолликуле только по его размеру, нельзя. Незрелая яйцеклетка, причины ее незрелости могут быть связаны с видом протокола, препаратами, используемыми при нем, состоянием яичников, не выявленными генетическими мутациями не всегда оплодотворяется. Есть разные гипотезы, почему яйцеклетка не оплодотворяется при ЭКО:
- недостаточное количество рецепторов на внешней оболочке ооцита, к которому должен прикрепиться сперматозоид для оплодотворения или их отсутствие;
- патологии блестящей оболочки, которые препятствуют проникновению сперматозоида, это может быть связано с наследственностью, мутациями;
- толстая внешняя оболочка ооцита, бывает у перезрелых яйцеклеток;
- другие факторы, которые не были учтены при подготовке к ЭКО, например, антиспермальные антитела у мужчины, не обнаруженные ранее, или технические накладки, когда ооциты извлекли, а сперму получили с опозданием.
Рекомендации врачей
Яйцеклетка в организме женщины жизнеспособна в течение 12—24 часов, а на питательных средах этот срок может сократиться. Чаще всего точно узнать, почему не оплодотворилась яйцеклетка при ЭКО не удается, так как еще не разработаны методы, позволяющие определить зрелость яйцеклетки до процедуры. Поэтому если не оплодотворилась яйцеклетка при ЭКО, то врачи рекомендуют в следующем протоколе делать ЭКО и ИМСИ. Конечно, можно пойти и другим путем, сделать следующее:
- пройти повторное обследование на антиспермальные антитела;
- сделать медико-генетические анализы;
- провести электронно микроскопическое исследование сперматозоида (ЭМИС);
- поменять протокол стимуляции, использовать для него другой препарат;
- исключить возможность технических проблем, сменить врача, клинику.
Конечно, все это сложно, многие анализы дорогостоящие и не всегда можно выявить истинную причину. А вот ИМСИ, это достаточно эффективный метод, с его помощью сразу исключается несколько причин, которые могли препятствовать оплодотворению, например, толстая внешняя оболочка ооцита, отсутствие рецепторов на ней. При проведении ИМСИ, вероятность оплодотворения возрастает и составляет 75—80%.
Так как во время ИМСИ генетический материал мужчины попадает непосредственно внутрь ооцита, остается только ждать, когда яйцеклетка начнет дробиться. К сожалению, даже ИМСИ не может быть гарантией получения эмбриона для подсадки. В некоторых случаях дробления не происходит и зигота погибает.
Если ЭКО с ИМСИ дает такой результат, то высока вероятность, что качество яйцеклеток у женщины низкое, есть какие-то патологии, которые еще не изучены специалистами. Единственный выход для таких пар, это использовать донорскую яйцеклетку. Многие женщины не хотят вынашивать и растить чужого для нее ребенка, но им необходимо понять, что если ооциты плохо оплодотворяются, вероятность того, что эмбрион, полученный из них, может иметь какие-то патологии, а использование ооцита донора позволит родить здорового ребенка.
 Эффективность ЭКО в многом зависит от того, как протекает эмбриологический этап: от качества полученных женских и мужских половых клеток, от того, как произошло оплодотворение яйцеклеток, а потом как происходит развитие эмбрионов при культивировании. На каждом этапе может произойти сбой, который явится причиной неудачи ЭКО. Рассмотрим основные моменты.
Эффективность ЭКО в многом зависит от того, как протекает эмбриологический этап: от качества полученных женских и мужских половых клеток, от того, как произошло оплодотворение яйцеклеток, а потом как происходит развитие эмбрионов при культивировании. На каждом этапе может произойти сбой, который явится причиной неудачи ЭКО. Рассмотрим основные моменты.
1. «Ооцитарный фактор» — это получение в цикле ЭКО яйцеклеток плохого качества. Общеизвестный факт, что с возрастом женщины качество ооцитов стремительно ухудшается.
У пациенток младше 35 лет, довольно редко, но также возможно получение яйцеклеток низкого качества. В таких ситуациях крайне сложно ответить на вопрос, с чем может быть это связано, но, как правило, с генетикой, с гормональной стимуляцией, эндометриозом, с различными эндокринными нарушениями (особенно часто с ожирением).
Сейчас активно ведутся исследования по изучению данного фактора бесплодия. Но, к сожалению, пока они не завершены и не имеют практического значения.
В случае установления ооцитарного фактора (а понять это возможно только при получении ооцитов при пункции фолликулов) предлагается замена протокола гормональной стимуляции, переход на ЭКО в естественном цикле. При неэффективности этих схем, переход на ЭКО с донорскими ооцитами.
Плохое качество сперматозоидов не так прямо связано с возрастом мужчины, больше с различными внутренними и внешними неблагоприятными факторами, но также может быть причиной неудач ЭКО.
2. Неправильное оплодотворение
В яйцеклетке и сперматозоиде в норме содержится по 23 хромосоме. В процессе оплодотворения в яйцеклетке формируется 2 клеточных ядра (пронуклеуса) — 2 pn — женское и мужское. Оплодотворённая яйцеклетка (зигота) содержит в норме 46 хромосом (23 от матери и столько же от отца).
Пронуклеусы в оплодотворённой яйцеклетке становятся видны через 12-14 ч после проникновения в неё сперматозоида. Через 19-22 часа пронуклеусы исчезают и формируется метафазная пластинка, а ещё через 3-4 часа начинается деление зиготы.
Послее дробления зиготы с аномалиями оплодотворения могут быть неотличимы от нормально оплодотворённых ооцитов. Поэтому наблюдение пронуклеусов имеет важное значение — по их количеству оценивается правильное формирование эмбриона.
Встречаются следующие патологии формирования пронуклеусов:
— 1 pn — присутствие в зиготе одного пронуклеуса может говорить об активации яйцеклетки без участия сперматозоида, реже — о слиянии ядер гамет и образование диплоидной зиготы с одним пронуклеусом;
— 3 pn — наличие 3-х пронуклеусов возможно при :
— * оплодотворении одной яйцеклетки 2-мя сперматозоидами;
— * формирование 3-го пронуклеуса из материала невыделившегося второго полярного тельца;
— * формирование 3-го пронуклеуса путём аномального формирования ядерной мембраны ;
— реже встречаются >3 pn.
ИКСИ (введение одного сперматозоида в цитоплазму яйцеклетки) не гарантирует правильного оплодотворения. Это объясняется главным образом сохранением второго полярного тела во время второго мейотического деления ооцита. Но 3 pn при этом варианте оплодотворения встречается реже, по разным данным ~ 2-3% против 8-12 % при оплодотворении методом ЭКО.
В неправильном оплодотворении могут играть роль следующие факторы:
— повышенные уровни эстрогенов в стимулированном цикле;
— продолжительность гормональной стимуляции;
— качество сперматозоидов;
— качество ооцита («гигантские» ооциты предрасположены к неправильному оплодотворению);
— поздний репродуктивный возраст женщины (по данным американских учёных H. J. Kang, Z. Rosenwaks частота оплодотворения и 3 pn достоверно выше у пациенток после 39 лет, несмотря на метод оплодотворения)
3. Остановка развития эмбрионов после правильного оплодотворения
В современных эмбриологических лабораториях процесс культивирования эмбрионов отработан до мелочей и тщательно соблюдается: индивидуальное культивирование эмбриона в планшетных инкубаторах; постоянный многоуровневый контроль условий культивирования; своевременная смена питательных сред, если культивирование происходит в двухступенчатых средах.
Поэтому при стабильных условиях культивирования, причину плохого развития остается искать только в качестве самого материала.
На остановку эмбриогенеза влияет качество как самих яйцеклеток, так и качество сперматозоидов.
Как правило, основное влияние на ход эмбриогенеза оказывает возраст родителей. Хотя и в молодом возрасте может наблюдаться снижение качества яйцеклеток, например, при эндометриозе, неясном генезе бесплодия. Причиной могут быть аномалии в хромосомном наборе самих родителей.
Принято считать, что до 3 дня развития эмбрион живет и развивается на материнских запасах, то есть, остановка или ухудшение развития до 3 суток указывает на плохое качество яйцеклетки.
На 3 сутки развития начинает работать сам геном эмбриона. И здесь добавляются факторы, привнесенные в эмбрион сперматозоидом. К сожалению, очень многие отклонения от нормы в качестве сперматозоидов и хроматина внутри них оказывают влияние на развитие эмбриона и могут вызывать анеуплоидии или недостаточность генома эмбриона. Качество конденсации и организации ДНК сперматозоида является важным фактором развития эмбриона, даже при выполнении ИКСИ.
Но есть данные, что некоторое количество материнской мРНК сохраняется до стадии бластоцисты и может также участвовать в остановке развития.
Хромосомные аномалии, несомненно, вызывают большой процент потерь эмбрионов. Генетические факторы регулируют скорость предимплантационного развития эмбриона. Существует тенденция к увеличению количества анеуплоидных эмбрионов с увеличением возраста. Большая часть анеуплоидий летальна для эмбриона на ранних стадиях развития. Но некоторые анеуплоидии не мешают эмбриону стать бластоцистой хорошего качества, например, при трисомии по 21 хромосоме, или синдроме Дауна.
В связи с этим, пациентам позднего репродуктивного возраста рекомендуется проведение предимплантационного генетического скрининга до переноса эмбриона в полость матки.
Кроме того, у пар более молодого возраста, если в нескольких циклах ЭКО при переносе эмбриона хорошего качества на стадии бластоцисты в однородный, достаточной толщины и хорошо кровоснабжающийся эндометрий беременность не наступает, необходимо выполнение предимплантационного генетического скрининга на все хромосомы. И, соответсвенно, переносить в полость матки эмбрион только с полным хромосомным набором.
 Трофимова Ольга Алексеевна Репродуктолог
Трофимова Ольга Алексеевна Репродуктолог
Кандидат медицинских наук
Заведующая Отделением ЭКО
Клиника «Мать и дитя» Юго-Запад
Другие статьи автора
-

Автор статьи — врач акушер-гинеколог, репродуктолог Клиники «Мать и дитя» Юго-Запад, Трофимова Ольга Алексеевна.
-

Автор статьи — врач акушер-гинеколог, репродуктолог Клиники «Мать и дитя» Юго-Запад, Трофимова Ольга Алексеевна.
Почему эмбрионы прекращают развиваться в лаборатории?
Если вы участвовали в протоколе ЭКО, то наверняка слышали от своего врача, что некоторые эмбрионы прекратили делиться. Некоторая часть пациенток так и не дожидается подсадки, так как все оплодотворенные яйцеклетки в конечном итоге прекращают развитие. Из-за чего это происходит? Можно ли предотвратить такой исход?
10-15% эмбрионов останавливаются в развитии на стадии деления 2-4 клетки. Некоторые даже не начинают процесс деления. Более половины всех замерших человеческих эмбрионов содержали хромосомные аномалии (генетические дефекты). Остановка деления – это естественный отбор, предотвращающий рождение потомства с генетическими аномалиями.
Почему не развивается эмбрион:
- неоптимальная среда развития;
- хромосомные аномалии;
- неспособность генома эмбриона активироваться;
- митохондриальные дефекты.
Когда эмбрионы оказываются в неоптимальной среде культивирования в лаборатории (например, из-за сбоя в работе инкубатора или инфицирования питательной среды), они могут перестать делиться. Если вам сообщили, что значительная часть эмбрионов перестала развиваться, поинтересуйтесь у эмбриолога, не вина ли это лаборатории. Пусть он покажет, как ведут себя эмбрионы других пациентов, помещенные в такие же условия.
Ооциты женщин старшего возраста имеют более высокий процент вероятности несения генетических дефектов, таких как анеуплоидия (неверное количество хромосом). Такие яйцеклетки после оплодотворения могут начать деление, но в зависимости от хромосомной аномалии рано или поздно их развитие остановится. Кто-то не преодолеет стадии зиготы, некоторые замрут в чашке Петри, кто-то – после подсадки в матку. Будут и такие, чье деление остановится лишь после имплантации (около 60% спонтанных абортов вызваны генетическими пороками). Генетические дефекты – самый распространенный фактор остановки развития эмбрионов.
При проникновении сперматозоида в яйцеклетку происходит оплодотворение и возникает эмбрион, который несет генетическую информацию как матери, так и отца. На первые сутки после слияния эмбрион представляет собой одну клетку. Тем не менее, вся информация, необходимая для превращения в полноценного ребенка, у него есть. Начальные несколько делений происходят благодаря информации, находящейся в цитоплазме яйцеклетки. С помощью только материнской стороны эмбрион дорастет до стадии 4-8 клеток и только затем активируется его собственный геном. Если по каким-либо причинам активация не произойдет, деление так и замрет на восьми клетках.
Эмбриону нужна энергия для деления. Ее вырабатывают специальные органеллы называемые митохондриями. Они несут свой собственный генетический материал и синтезируют аденозинтрифосфат (АТФ). АТФ – универсальный источник энергии для клеток, которую они тратят, в том числе, на деление. Так как митохондрии находятся в цитоплазме, эмбрион получает их только от матери. Митохондрии спермиев сразу после оплодотворения уничтожаются. Чем старше женщина, тем больше вероятность накопления дефектов в митохондриях. Это влияет на их функции, в том числе на выработку АТФ. Оказавшись на «голодном пайке», клетки не смогут продолжать деление. Эта гипотеза подтвердилась на опытах — когда в яйцеклетку женщины старшего возраста вводилась цитоплазма молодой девушки, эмбрион начинал делиться. Сейчас такой метод используется при проведении ЭКО. Уже родились дети, эмбрионы которых подвергались цитоплазматическому переносу.
Если эмбрион перестал развиваться in vitro, есть ли способ запустить деление вновь? К сожалению, нет. Важно правильно задокументировать, когда и (возможно) почему он перестал делиться. Это необходимо для выбора дальнейшей тактики лечения и ведения пациентки.
Далеко не все ооциты, полученные после стимуляции, оплодотворятся; не все эмбрионы будут достаточного качества, чтобы быть перенесенными в матку; и не все подсаженные станут детьми.
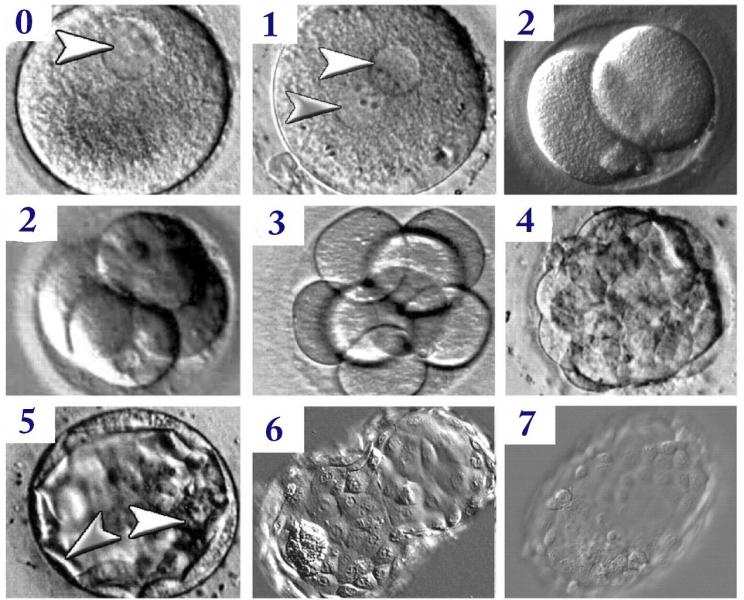
Развитие эмбриона после ЭКО от 0 до 7 дня (0-7). После оплодотворения клетка претерпевает серию митотических делений. Стрелками в нулевом и первом днях помечены гаплоидные ядра зиготы. На четвертый день эмбрион становится более компактным и называется морулой, состоящей из клеток (бластомеров), окруженных так называемой «блестящей оболочкой» (гликопротеиновой оболочкой). Бластоциста, формируемая на пятый день, — полая структура, состоящая из внутренней клеточной массы (указана белой стрелкой) и трофобласта (серая стрелка). На шестой день бластоциста выходит из блестящей оболочки. Имплантация эмбриона при ЭКО в стенку матки происходит на седьмой день.
>Как «ребенок из пробирки» выглядит в пробирке?
/О беременности/Планирование беременности. ЭКО/ЭКО
День 5
Морула меняется не по дням, а по часам. Вскоре половина ее объема составляет полость, а клетки, из которых она состоит, состоят из внешнего слоя трофобласта (он отвечает за внедрение в ткань матки и образование плаценты) и плотной клеточной массы – собственно, будущего малыша. Теперь это уже не морула, а бластоциста. При естественном течении беременности полость бластоцисты медленно расширяется, внешняя оболочка рвется, и начинается процесс имплантации, на который потребуется еще день или два.
” Ученые до сих пор не пришли к единому мнению, почему при искусственном оплодотворении до стадии бластоцисты «доживает» только около 40% эмбрионов: виной ли тому искусственная среда обитания, или это проявление генетической неполноценности некоторых из них. Но, в любом случае, выживают только лучшие из лучших, да и среди них врачи продолжают вести тщательный отбор. На этот раз – посредством генетического анализа: эмбрион уже достаточно велик, чтобы можно было изъять из него несколько клеток и проверить на генетические заболевания.
Когда лучше подсаживать эмбрион?
Подсадка возможна в любой день, с первого по шестой, и каждого выбора есть свои плюсы и минусы. Если поместить эмбрион в матку рано, на первый или второй день, то возможное негативное влияние искусственной среды будет минимизировано, но ведь и полость матки на таком сроке для будущего малыша не «дом родной», он должен был бы еще находиться в маточной трубе! К тому же на таком сроке еще невозможно оценить ни качество эмбриона, ни его подверженность генетическим заболеваниям.
На третий день можно уже уверенно отсеять нежизнеспособные эмбрионы, однако, для генетического анализа по-прежнему еще очень рано.
На четвертый, а особенно на пятый день оценить можно все: и жизнеспособность эмбриона, и генетические заболевания, которые он унаследовал. Наконец, именно в этот момент естественно зачатый малыш, а вернее – бластоциста, из которой он вы итоге разовьется, оказывается в полости матки. Так что именно в этот момент подсадка эмбриона наиболее удобна и естественна.
Плохо то, что к этому моменту искусственно оплодотворенные яйцеклетки уже несколько дней борются за жизнь «в пробирке» и больше половины в ходе этого жестокого соревнования «сходят с дистанции». Среди неудачников не только жертвы генетических мутаций, но и вполне здоровые и качественные эмбрионы, которые по неизвестным причинам замирают и останавливаются в своем развитии. Так что к часу «Х» может попросту не дожить ни один эмбрион.
” Так что врачи при выборе дня имплантации руководствуются целым рядом критериев. Если ранее уже были неудачные попытки ЭКО, то обычно пытаются перенести в полость матки «более юные» эмбрионы – третьего или даже второго дня развития, надеясь, что в естественной среде их выживаемость будет выше. Если существует вероятность генетических заболеваний, то подсадку эмбриона стараются оттянуть до того момента, когда будут сделаны достоверные анализы.
Именно поэтому, хотя идеальным днем для подсадки мог бы стать день №4, ее осуществляют только на следующий день, или даже через день.
Наконец, еще один фактор, который приходится учитывать, — психологическое состояние мамы. Чем дольше она ждет переноса эмбриона, тем больше нервничает, и тем меньше шансы на удачную берменность.
Дорогие будущие мамы! Не нервничайте! Мы верим — все у нас получится!











