Шмыров О.С.
Пузырно-мочеточниковый рефлюкс (ПМР) — это ретроградный ток (заброс) мочи из мочевого пузыря в мочеточник. ПМР воздействует отрицательно на почку, создавая условия для активизации инфекции мочевых путей и хронического пиелонефрита, а также вызывает патологические изменения ткани почки со снижением её функции — рефлюкс нефропатию.
Моча, образуясь в ткани почки, далее попадает в почечную лоханку, из лоханки — в мочеточник, из мочеточника — в мочевой пузырь. В мочевом пузыря моча накапливается (фаза накопления мочи), и при сокращении мочевого пузыря выводится наружу через мочеиспускательный канал (фаза изгнания мочи).В норме, моча течёт только в направлении «от почки к мочеиспускательному каналу», что обеспечивается волнообразными сокращениями мышечных волокон лоханки и мочеточника, и наличием функционального клапана в месте впадения мочеточника в мочевой пузырь. Пузырно-мочеточниковый рефлюкс — заболевание, при котором ток мочи приобретает обратное направление, вследствие несостоятельности клапанного механизма пузырно-мочеточникового сегмента, т.е. моча забрасывается в мочеточник в фазу накопления мочи (пассивный рефлюкс), в фазу изгнания мочи (активный рефлюкс) или в обе фазы (смешанный рефлюкс).
Синонимами термина «пузырно-мочеточниковый рефлюкс» являются: пузырно-почечный рефлюкс и пузырно-лоханочный рефлюкс.
Основной опасностью существования пузырно-мочетоикового рефлюкса (ПМР) является рецидивирующая инфекция мочевыхпутей и рефлюкс- нефропатия, приводящие к ухудшению функции почки, или даже, в тяжёлых случаях, к потере функции почки.
Под термином «рефлюкс-нефропатия» понимают комплекс склеротических изменений в структуре почки, приводящих к замещению паренхимы почки — патологической соединительной тканью,неспособной выполнять почечную функцию.
Наиболее частым проявлением пузырно-мочеточникового рефлюкса является инфекция мочевых путей, в виде:
- лейкоцитурии (увеличение количества лейкоцитов в анализе мочи)
- пиелонефрита (повышение температуры тела, недомогание, увеличение количества лейкоцитов в анализе мочи, иногда боли в поясничной области)
Если у ребёнка любого возраста отмечается устойчивое увеличение количества лейкоцитов в анализе мочи — первое состояние, которое нужно диагностировать — ПУЗЫРНО-МОЧЕТОЧНИКОВЫЙ РЕФЛЮКС.
На первом этапе диагностики выполняется ультразвуковое исследование почек, мочеточников и мочевого пузыря. При расширении лоханки почки и мочеточника может быть заподозрен пузырно-мочеточниковый рефлюкс. При наличии признаков истончения паренхимы почек — требуется проведение дополнительного исслеования — ультразвуковой допплерографии почек. УЗДГ почек позволит выявить признаки рефлюкс-нефропатии.
Так же на начальном диагностическом этапе выявляются варианты дисфункции мочевого пузыря, которые могут быть причиной и(или) усугублять течение пузырно-мочеточникового рефлюкса, путём регистрации ритма спонтанных мочеиспуканий, выполнения УЗИ с полным и опорожнённым мочевым пузырём, функциональных исследований мочевого пузыря в случае необходимости.
Основным способом диагностики ПМР является микционная цистография.
Микционная цистография заключается в введении раствора, содержащего контрастное вещество в мочевой пузырь (через катетер) и выполнении рентгеновских снимков до и во время мочеиспускания. Если отмечен заброс контрастного вещества в мочеточник и лоханку почки — диагностируется ПУЗЫРНО-МОЧЕТОЧНИКОВЫЙ РЕФЛЮКС.
В зависимости от уровня ретроградного заброса контрастноговещества на цистографии и сопутствующих изменений размеров мочеточника и почечной лоханки разделяют 5 степеней ПМР (внутренняя ссылка):
- 1 степень — на цистографии контрастируется только нерасширенный мочеточник;
- 2 степень — контрастируется мочеточник и почечная лоханка, не расширены;
- 3 степень — мочеточник и лоханка незначительно расширены;
- 4 степень — контраст определяеся в умеренно извитом, расширенном мочеточнике и расширенной почечной лоханке;
- 5 степень — контрастируется коленообразно извитой, расширенный мочеточник и расширенная коллекторная система почки.
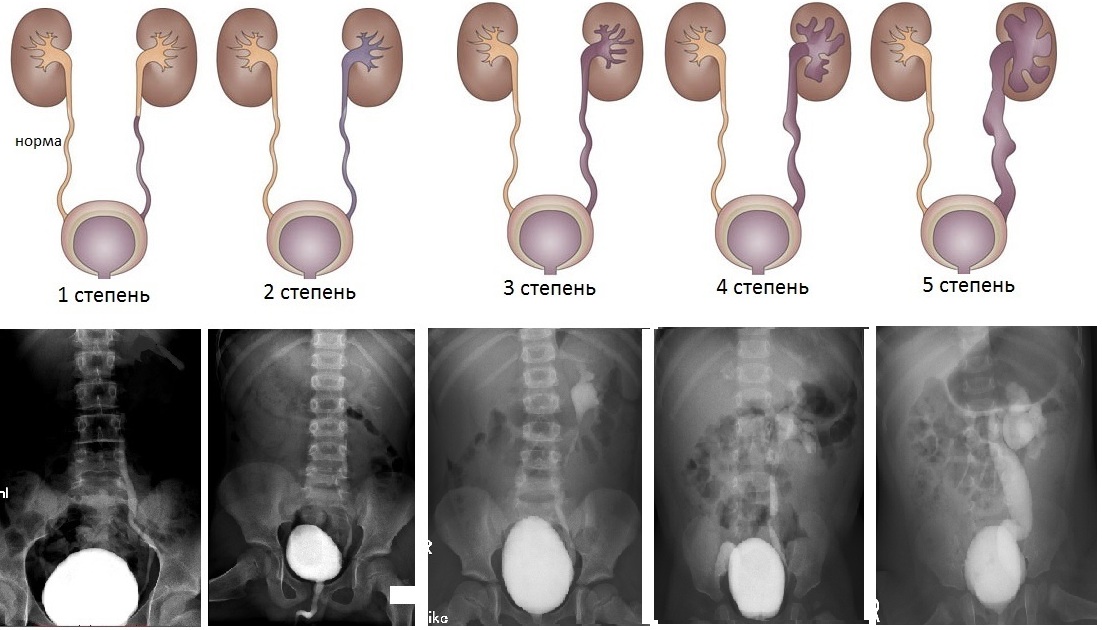 Рис.1 Градация пузырно-мочеточникового рефлюкса по степеням, в зависимости от уровня заброса контрастного вещества на цистографии.
Рис.1 Градация пузырно-мочеточникового рефлюкса по степеням, в зависимости от уровня заброса контрастного вещества на цистографии.
В ряде случаев, с целью исключения сопутствующих пороков верхних мочевых путей необходимо выполнение экскреторной урографии (введения контрастного вещества внутривенно и последующим выполнением серии рентгеновских снимков, с целью визуализации структуры лоханки почки и мочеточника и для выявления нарушения эвакуации контрастного вещества из верхних мочевых путей).
С целью оценки функции почек и выраженности рефлюкс-нефропатии выполняется радиоизотопное исследование почек — статическая нефросцинтиграфия.
Цистоскопия — инструментальное исследование, которое выполняется на этапе выбора тактики лечения. Технология выполнения цистоскопии: Через мочеиспускательный канал в полость мочевого пузыря вводится ЦИСТОСКОП — оптический прибор, имеющий вид стержня — трубки, диаметром от 1,2 до 4 мм (подбирается в зависимости от возраста), подключённый к видеокамере и экрану. Через цистоскоп осматривается полость мочевого пузыря, слизистая и устья мочеточников — отверстия, которыми открываются мочеточники в полость мочевого пузыря. Визуальная анатомия устьев мочеточников оказывает влияние на выбор тактики лечения пузырно-мочеточникового рефлюкса.
На выбор тактики лечения оказывает влияние степень рефлюкса, активность инфекции мочевых путей (как часто возникают изменения в анализе мочи и(или)обострение пиелонефрита), выраженность признаков рефлюкс-нефропатии и цистоскопическая анатомия устьев мочеточников.
При первой и второй степени рефлюкса показана консервативная терапия (средства направленные на профилактику инфекции мочевых путей, на улучшение трофики мочевого пузыря, физиотерапия). Только при неэффективности терапии и персистенции инфекции мочевых путей рассматривается вопрос об эндоскопической инъекционной коррекции ПМР.
При третьей степени рефлюкса частота перехода от консервативной терапии к инъекционной коррекции выше. У части пациентов с прогрессирующей нефропатией, рецидивирующей инфекцией мочевых путей и нарушением эндоскопической анатомии устьев мочеточников целесообразно выполнение хирургического вмешательства для ликвидации ретроградного заброса мочи — антирефлюксной операции — реимплантации мочеточников.
При четвёртой и пятой степени рефлюкса эффективность эндоскопической инъекционной коррекции существенно ниже, чем при меньших степенях и используется ограниченно, при невыраженных нарушениях эндоскопической анатомии устьев мочеточников. Наибольшее значение при высоких степенях ПМР приобретают варианты оперативного лечения — антирефлюксные операции Лич-Грегуара, Политано-Леадбеттера, Коэна, Барри.
Содержание
Описание способов коррекции ПМР
Эндоскопическая инъекционная коррекция пузырно мочеточникового рефлюкса заключается в введении гелевого импланта через специальную иглу в область устья мочеточника во время цистоскопии.
Введённый имплант формирует «бугорок», который при отсутствии выраженных изменений анатомии устья обеспечивает «функциональный клапан» и препятствует забросу мочи из мочевого пузыря в мочеточник.
Существуют различные типы имплантов — биодеградируемые (рассасывающиеся), частично биодеградируемые и небиодеградируемые (нерассасывающиеся). При выборе импланта специалист руководствуется множеством различных факторов — активностью инфекции, возрастом, степенью рефлюкса, анатомией устьев — и осуществляет его (выбор) индивидуально дифференцированно.
Оперативное лечение пузырно-мочеточникового рефлюкса сохраняет свою актуальность для высоких степеней ПМР и в случае неудачных эндоскопических инъекционных коррекций, заключается в реимплантации мочеточников в мочевой пузырь с хирургическим формированием антирефлюксного механизма.
Предложено множество открытых оперативных методик формирования антирефлюксного механизма через разрез передней брюшной стенки и мочевого пузыря. Самые распространённые и часто используемые: уретероцистонеоимплантации по Коэну (Cohen), Лич-Грегуару (Lich-Gregoir), Политано-Леадбеттеру (Politano-Leadbetter), Барри (Barry).
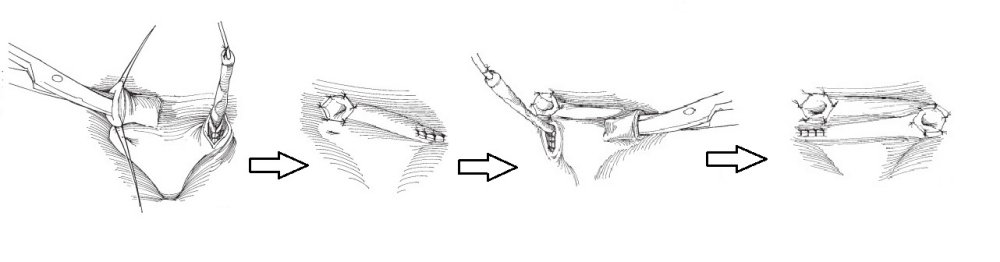 Рис.2 Транстригональный способ уретероцистонеоимплантации по Коэну (Cohen)
Рис.2 Транстригональный способ уретероцистонеоимплантации по Коэну (Cohen)
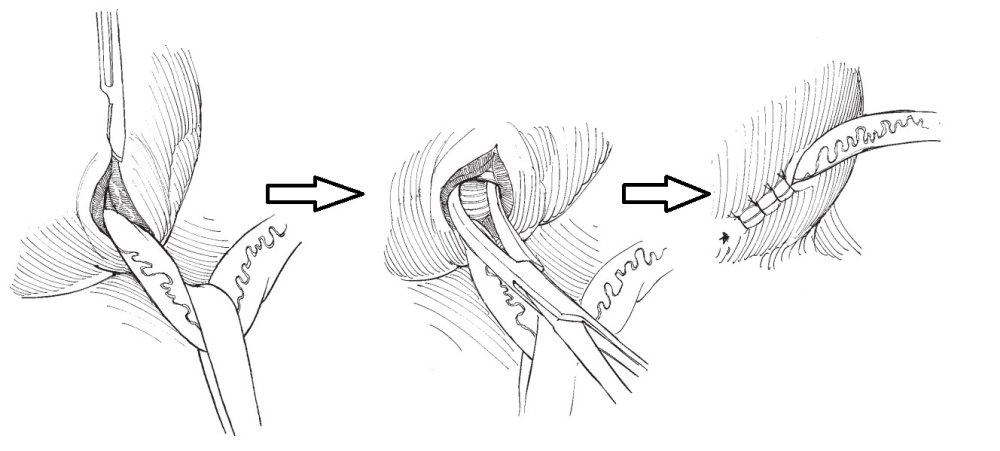 Рис.3 Экстравезикальное формирование антирефлюксного тоннеля по Лич-Грегуар (Lich-Gregoir)
Рис.3 Экстравезикальное формирование антирефлюксного тоннеля по Лич-Грегуар (Lich-Gregoir)
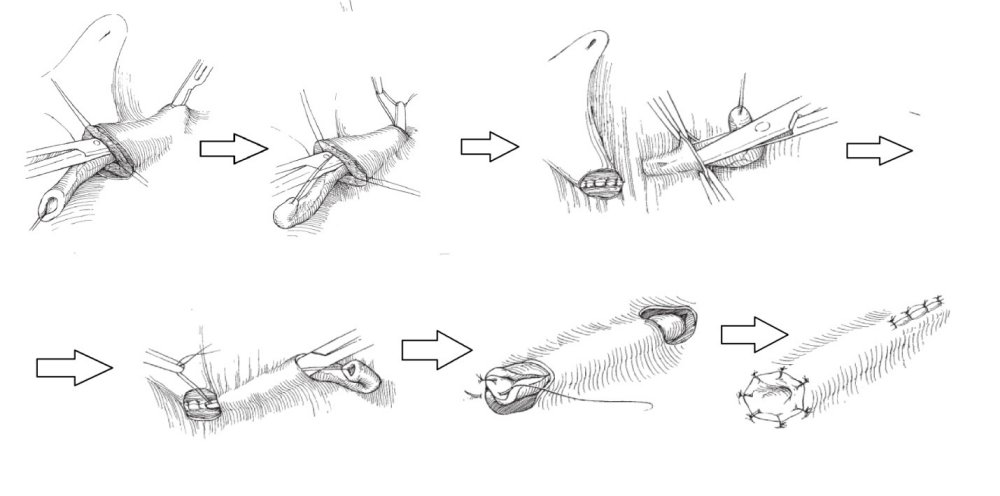 Рис.4. Интра-экстравезикальный способ Политано-Леадбеттера (Politano-Leadbetter)
Рис.4. Интра-экстравезикальный способ Политано-Леадбеттера (Politano-Leadbetter)
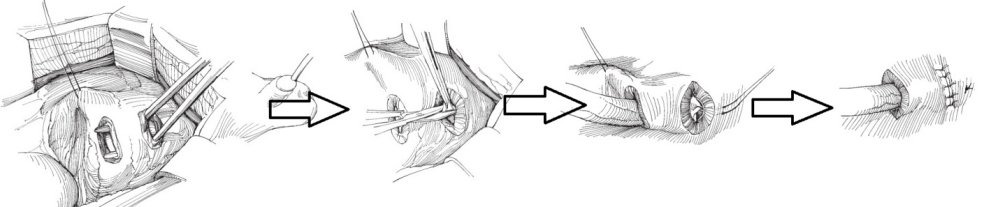 Рис.5. Экстравезикальный уретероцистонеоанастомоз по Барри (Barry)
Рис.5. Экстравезикальный уретероцистонеоанастомоз по Барри (Barry)
С ними Вы можете подробнее ознакомиться в любом руководстве по урологии. В нашей статье мы опишем своё «ноу-хау» — модификации открытых методик, которые мы выполняем лапароскопически или везикоскопически — через проколы передней брюшной стенки и мочевого пузыря, без больших разрезов, малотравматически.
Везикоскопическая уретроцистонеоимплантация по Коэну (Cohen). Выполняется в нашем отделении при высоких степенях рефлюкса с нарушением анатомии устья мочеточника, в том числе после неудачных инъекционных эндоскопических коррекций.
Через 3 прокола передней брюшной стенки в полость мочевого пузыря вводится лапароскоп и два эндоскопических инструмента. Мочеточник мобилизовывается в полости мочевого пузыря, затем формируется подслизистый тоннель в поперечном направлении. Длина тоннеля, согласно классическим представлениям, подтвердившим свою эффективность должна быть в 4 раза больше диаметра мочеточника. Мобилизованный отдел мочеточника перемещается в подслизистый тоннель. Неоустье (новое устье) фиксируется по окружности мочеточника 5-6 узловыми швами тонкой, саморассасывающейся нитью на атравматичной игле. Затем ушиваются оставшиеся дефекты слизистой мочевого пузыря, троакары удаляются.
Лапароскопическая операция выгодно отличается ототкрытой более лёгким протеканием послеоперационного периода, отличным косметическим эффектом (нет разреза) и более быстрой выпиской из стационара (5-8 дней).
Лапароскопическая операция Лич-Грегуара (Lich-Greoir). Выполняется в нашем отделении при 3 и 4 степени рефлюкса при неэффективности эндоскопических коррекций, типичной локализации устья мочеточника, когда требуется создание дополнительной антирефлюксной защиты.методика применяется преимущественно у мальчиков (у девочек расположение матки и её кровеносных сосудов может препятствовать применению способа).
Через три троакара в брюшную полость вводится лапароскоп и два эндоскопических инструмента. Мобилизуется дистальный отдел мочеточника, рассекается мышечный слой мочевого пузыря. На слизистую мочевого пузыря укладывавется мочеточник и над ним сшивается рассечённый мышечный слой мочевого пузыря — формируется антирефлюксный механизм.
Лапароскопическая модификация операция Политано-Леадбеттера подразумевает под собой сохранение направления хода мочеточника по направлению к шейке мочевого пузыря. Это делает её предпочтительной у пациентов с мочекаменной болезнью в анамнезе, так как предоставляет возможность для эндоскопического удаления или дробления камней в просвете мочеточника. В мочевой пузырь через переднюю брюшную стенку устанавливаются 3 троакара, мочеточник мобилизовывается внутрипузырно. Слизистая мочевого пузыря рассекается по направлению к шейке мочевого пузыря. На мышечный слой укладывается мочеточник, швами фиксируется устье, рассечённая слизистая мочевого пузыря сшивается над мочеточником — формируется антирефлюксная защита.
Лапароскопическая экстравезикальная уретероцистонеоимплантация (модификация операции Barry) незаменима при необходимости изолированной реимплантации рефлюксирующего мочеточника нижнего сегмента при удвоении почек. Методика предотвращает травматизацию мочеточника верхнего, неповреждённого сегмента.
В брюшную полость устанавливаются три тоакара, над дистальными отделами удвоенных мочеточников вскрывается брюшина и порочный мочеточник нижнего сегмента отделяется от нормального мочеточника верхнего сегмента. Со стороны брюшной полости мышечный слой мочевого пузыря рассекается в поперечном направлении до слизистой. В сформированное ложе укладывается дистальный отдел мочеточника, перфорируется слизистая, узловыми швами формируется устье, а мышечный слой сшивается над мочеточником — создаётся антирефлюксный механизм.
Все описанные оперативные методики являются ультрасовременными, и освоены далеко не во всех клиниках России и стран развитого капитализма. В нашем отделении выполнено более 30 подобных операций. Какую методику применить в конкретном случае мы каждый раз решаем коллегиально, оценивая данные обследования и все необходимые аспекты описанные Выше. На момент публикации этого текста у наших пациентов, перенёсших лапароскопические или везикоскопические антирефлюксные операции по поводу пузырно-мочеточникового рефлюкса РЕЦИДИВОВ или других осложнений, характерных для открытых методик, НЕТ.
Дети быстрее восстанавливаются, болевой синдром минимален, соответственно выписываются домой раньше.
Отделение плановой хирургии и урологии андрологии
Морозовская детская городская клиническая больница
Москва, 2014
УЗИ сканер HS50
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Введение
Воспалительные заболевания почек и мочевыводящих путей — одни из самых распространенных заболеваний детского возраста. Предрасполагающими факторами, на фоне которых наиболее часто развиваются эти изменения, могут быть различные анатомические аномалии органов мочевой системы, например патология мочеточника и пиелоуретрального сегмента, нарушающие нормальную выделительную функцию почки, изменения со стороны пузырно-мочеточникового сегмента, приводящие к нарушению уродинамики, изменения со стороны почечных сосудов, нарушающие кровоснабжение почки. Перечисленные изменения при воздействии экзогенного фактора (переохлаждение) способствуют развитию воспалительных изменений в паренхиме почки и мочевыводящих путей.
Цель настоящего исследования — определение диагностической тактики и последовательности применения различных методов лучевой диагностики у детей с воспалительными заболеваниями почек и мочевыводящих путей, сравнение эффективности данных методов в диагностике различной уронефрологической патологии.
Материалы и методы
Обследовано 176 детей в возрасте от 2 до 14 лет, 52,8 % составили девочки, 47,2 % — мальчики. УЗИ с цветным допплеровским картированием (ЦДК) проводили на современных ультразвуковом (с использованием конвексного датчика с диапазоном частот 3,5-5 Мгц) и рентгенологическом аппаратах, а радионуклеидные исследования — на сцинтилляционной гамма-камере «СЦИНТИПРО».
Из 176 пациентов 18 потребовалось только проведение УЗИ с ЦДК с назначением последующей динамики УЗИ. Остальным 158 пациентам после проведения УЗИ с ЦДК были необходимы другие лучевые методики. Диагностировалась следующая патология: начальные проявления воспалительных изменений — у 133 детей, развернутая картина при воспалительных изменениях в почках и мочевыводящих путей — у 21 ребенка, «маленькая» почка — у 4 пациентов (у 3-гипоплазированная, у 1 — сморщенная). Кроме того, у 8 пациентов выявлен нефроптоз, у 2 -тазовая дистопия почки, у 2 -ротация почек. Неполное удвоение полостной системы диагностировано в 11 наблюдениях, полное — в 1 наблюдении. Кисты определены у 3 детей, кальцинат — у 1, ангиолипома — у 1 ребенка. Симптом Фролея на экскреторной урографии определялся у 17 человек, патология мочеточника (стриктура, высокое отхождение, клапан, перегиб) — у 8 детей.
УЗИ с ЦДК позволило установить у 25 пациентов обеднение сосудистого рисунка на фоне «маленькой» почки и развернутой картины воспалительных изменений; у 9- различную сосудистую патологию (наличие добавочного сосуда, удвоение, стеноз, изгиб почечной артерии). У 1 пациента была диагностирована артериовенозная мальформация.
Результаты и обсуждение
Наиболее популярным способом диагностики и контроля пузырно-мочеточникового рефлюкса до сих пор считается восходящая цистография, главные достоинства которой заключаются в получении информации о деталях строения мочевого пузыря и анатомии уретры, а также в возможности классифицировать пузырно-мочеточниковый рефлюкс в соответствии с классификацией Heikel-Parkkulainenb (1966), в основе которой лежит оценка степени выраженности забрасывания рентгеноконтрастного вещества при выполнении восходящей цистографии.
Пузырно-мочеточниковый рефлюкс делится на активный- возникает в момент мочеиспускания, т.е. в момент сокращения детрузора, и пассивный — когда имеется постоянное свободное соединение мочевого пузыря с содержимым мочеточника, существуют и смешанные формы рефлюкса (активно-пассивные) (рис. 1).
Рис. 1. Восходящая цистография. Активно-пассивный пузырно-мочеточниковый рефлюкс слева 4 степени. Выраженная дилатация чашечно-лоханочной системы, деформация чашечек.
а) В фазе максимального наполнения мочевого пузыря, пассивный рефлюкс.
б) В фазе мочеиспускания, активный рефлюкс.
Однако существенная лучевая нагрузка при восходящей цистографии, особенно опасная для девочек, заставляет искать альтернативные подходы к диагностике пузырно-мочеточникового рефлюкса. Кроме того, рентгеновский метод не может гарантировать, что пузырно-мочеточниковый рефлюкс, проявления которого в немалых случаях весьма ограничены по времени (секундами), непременно совпадет с моментами выполнения снимков. Одними из таких альтернативных методов являются УЗИ с ЦДК и радионуклеидная цистография . УЗИ с ЦДК позволяют получать изображение движения потоков мочи, оценивать количественные и качественные характеристики выбросов, которые зависят от состояния транспортной функции мочевых путей.
Признаками пузырно-мочеточникового рефлюкса при УЗИ с ЦДК являются: дилатация мочеточника в нижних и верхних отделах при среднем или максимальном наполнении мочевого пузыря и стабильное расширение лоханки более 10 мм, независимо от наполнения мочевого пузыря (рис. 2). Если после микции лоханка не уменьшилась или даже увеличилась в размерах, то имеет место активный рефлюкс, при уменьшении лоханки в размерах диагностируется пассивный рефлюкс.
Рис. 2. Эхограммы на фоне мочевого пузыря.
а) Эхограмма расширения полостной системы почки.
б) Эхограмма расширенного мочеточника.
1 — мочевой пузырь, 2 — мочеточник.
Кроме того, при наличии пузырно-мочеточникового рефлюкса УЗИ с ЦДК может определить: уменьшение размеров почки на стороне поражения; циклическое изменение диаметра мочеточника в верхнем и (или) нижнем отделах; допплерографическую регистрацию обратного тока мочи в мочеточнике в виде одногорбой кривой со снижением всех количественных показателей; вертикальную направленность мочеточниково-пузырного выброса, который в норме имеет направление под углом 30-40° по отношению к условной линии, соединяющей устья мочеточников (рис. 3).
Метод радионуклеидной цистографии был внедрен Winter в 1959 г. . Существует две формы: прямая, при которой изотопы вводятся трансуретрально в мочевой пузырь и непрямая радионуклеидная цистография, основным принципом которой является способность почки в короткий срок выделить все количество внутривенно введенного радиоизотопа. Зоны интереса определяют вокруг каждой почки и мочевого пузыря и строят кривые «время-активность» . При подозрении на небольшой рефлюкс формируют дополнительные зоны интереса в области каждого мочеточника. В своем исследовании мы использовали метод непрямой радионуклеидной цистографии.
Признаками пузырно-мочеточникового рефлюкса при непрямой радионуклеидной цистографии являются: повторное усиление контрастирования чашечно-лоханочной системы (ЧЛС) на соответствующей стороне во время микционной пробы; формирование на ренограмме резкого подъема кривой вверх, вслед за которым после пробы, вновь увеличивается радиактивность над областью мочевого пузыря в связи с возвращением в просвет последнего рефлюксированной мочи (рис. 4), (табл. 1).
Рис. 4. Ренограмма пузырно-мочеточникового рефлюкса при радионуклеидной непрямой цистографии.
а) Пузырно-мочеточниковый рефлюкс отсутствует.
б) Двухсторонний активный пузырно-мочеточниковый рефлюкс.
А — правая почка; В — правый мочеточник; С — левая почка; D — левый мочеточник. Таблица 1. Сравнение методов лучевой диагностики по выявлению пузырно-мочеточникового рефлюкса (ПМР).
| Метод диагностики | Количество | |
|---|---|---|
| исследований | выявленных ПМР | |
| Непрямая радионуклеидная цистография | 64 | 17 (26,6 %) |
| УЗИ с ЦДК | 176 | 43 (24,4 %) |
| Восходящая цистография | 60 | 4 (6,7 %) |
Из табл. 1 видно, что восходящая цистография имеет самый низкий процент диагностики пузырно-мочеточникового рефлюкса, непрямая радионуклеидная цистография и УЗИ с ЦДК имеют примерно одинаковый процент выявления данной патологии. Следует отметить, что 4 пациентам, у которых диагностирован пузырно-мочеточниковый рефлюкс при восходящей цистографии, предварительно было выполнено УЗИ с ЦДК и непрямая радионуклеидная цистография, выявившие у 3 из них признаки пузырно-мочеточникового рефлюкса.
Изменения, выявляемые методами лучевой диагностики у детей при воспалительных заболеваниях почек и мочевыводящих путей, могут быть условно разделены на три группы: начальные проявления (минимальные изменения, которые определяются лучевыми методами диагностики), развернутая картина воспалительных изменений и диагностика «маленькой» почки (имеется ввиду гипоплазированная, или сморщенная почка).
Необходимо отметить, что изменения со стороны почек и мочевыводящих путей, которые выявляются при УЗИ с ЦДК и при динамической ангионефросцинтиграфии не специфичны для того или иного заболевания, а характеризуют структурные изменения и нарушения функциональных способностей мочевыделительной системы. Диагнозы пиелонефрита или гломерулонефрита являются, на наш взгляд, в первую очередь клиническими, постановка их возможна только при совокупности синдромов: клиническая картина, данные физикального обследования, изменения в анализах и, конечно изменения, которые определяются лучевыми методами диагностики.
УЗИ позволяет выявить изменения в серошкальном режиме, а в сочетании с ЦДК детально охарактеризовать кровоток в отдельных участках сосудистого русла почки и установить, если имеется, сосудистую патологию .
В начальном периоде воспалительных изменений УЗИ с ЦДК выявляет умеренно выраженные диффузные изменения паренхимы почки на фоне сохранения четкости кортико-медуллярной дифференцировки (КМД); контуры почек сохранены, четкие, ровные; невыраженная дилатация лоханки (без истончения паренхимы); интраренальный сосудистый рисунок почки сохранен; скоростные показатели артериального ренального кровотока сохраняются в пределах нормы.
При развернутой картине УЗИ с ЦДК характеризуется неровностью, нечеткостью, деформацией контура почки, который местами может не прослеживаться; почка иногда местами плохо дифференцируется от окружающих тканей, что затрудняет определение ее размеров; визуализируются мелкие, неправильной формы втяжения контура, распределенные либо по всему контуру, либо в каком-то фрагменте почки; определяется нечеткость кортико-медуллярной дифференцировки; имеются выраженные диффузные изменения паренхимы почки с умеренным неравномерным повышением ее эхогенности; дилатация чашечно-лоханочной системы; фрагментарное истончение паренхимы почки с компенсаторным утолщением или сохранением толщины других ее участков (рис. 5); умеренное обеднение интраренального сосудистого рисунка, наиболее выраженное в местах деформации и втяжения контура почки; снижение скоростных характеристик артериального кровотока (рис. 6).
Рис. 5. Эхограмма почки.
а) Воспалительные изменения в почке.
б) Втяжение на контуре почки (стрелка).
Рис. 6. УЗИ почки при воспалительных изменениях в режиме ЦДК.
а) Интраренальный сосудистый рисунок почки сохранен, кортикальный кровоток определяется во всех отделах паренхимы.
б) Обеднение сосудистого рисунка.
в) Скоростные показатели в устье почечной артерии в пределах возрастной нормы: Vps — 83,7 см/с; Ved — 34,1 см/с; RI — 0,63; PI — 0,96.
При наличии у ребенка «маленькой» почки УЗИ с ЦДК определяет уменьшенную в размерах почку с нарушением правильности ее контуров, почка с трудом дифференцируется от окружающих тканей; резко нарушена или отсутствует кортико-медуллярная дифференцировка; визуализируются диффузные неравномерные изменения паренхимы почки с гетерогенным повышением эхогенности; дилатация чашечно-лоханочной системы; выраженное обеднение сосудистого рисунка пораженной почки со снижением скоростных характеристик артериального ренального кровотока (рис. 7, 8).
Рис. 7. Эхограмма гипоплазии почки.
а) В-режим.
б) Режим ЦДК.
в) Режим ЦДК.
Гемодинамические показатели артериального кровотока в почечной артерии: Vps — 54 см/с, Ved — 22 см/с, RI — 0,4, PI — 0,7. Рис. 8. Эхограмма сморщенной почки.
а) В-режим.
б) Режим ЦДК.
УЗИ с ЦДК позволяет определить и различную сосудистую патологию. Артериовенозные мальформации (рис. 9, 10), наличие добавочных сосудов, удвоения, изгибы и стенозы почечной артерии (рис. 11), все эти изменения приводят к нарушению кровоснабжения почки, и в определенных условиях способствуют развитию воспалительных изменений в почках. Кроме того, это часто может служить причиной ренальной артериальной гипертонии. Динамическая ангионефростинтиграфия позволяет изучить раздельную и суммарную функциональную способность почек, уродинамику верхних мочевых путей, анатомо-топографические особенности почек. Построение кривых «активность-время», имеющих вид ренограмм с сосудистым, функциональным (либо фильтрационным, либо секреторным) и экскреторными сегментами, также позволяет судить о поглотительной и выделительной функции каждой почки. Начальные признаки нарушения функциональной способности почек при динамической ангионефростинтиграфии проявляются в виде удлинения времени канальцевой секреции (Тmax) и замедления экскреции (Т1/2) из-за воспалительной инфильтрации межуточной ткани со снижением тонуса чашечно-лоханочной системы и нередко мочеточника.
Рис. 9. УЗИ в режиме ЦДК артериовенозной мальформации.
в) Кровоток в почечной артерии вне зоны мальформации: Vps — 191 см/с, Ved — 186 см/с, RI — 0,1, РI — 0,1.
Рис. 10. Серия ангиограмм.
а) Нефроартериография левой почки.
б) Нефроартериография левой почки.
в) Нефроартериография левой почки.
г) Нефроартериография правой почки.
Визуализируется массивный артериовенозный сброс слева с резким обеднением внутрипочечного сосудистого рисунка. Почечная вена слева расширена, деформирована. В среднем и верхнем сегментах слева негомогенное образование округлой формы с неровными нечеткими контурами диаметром 5 см. При контрастировании образование высокой интенсивности. Рис. 11. УЗИ в режиме ЦДК.
а) Эхографическая картина извитости почечной артерии (стрелка) с обеднением сосудистого рисунка почки.
б) Эхографическая картина извитости почечной артерии (стрелка) с обеднением сосудистого рисунка почки.
в) Стеноз почечной артерии: 79,1%.
г) Две почечные артерии в воротах почки.
д) Две почечные артерии в воротах почки и сосудистое дерево почки.
При развернутой картине поражения почек и мочевыводящих путей на динамической ангионефростинтиграфии определяется снижение амплитуды ренограммы (Аmax) по сравнению с коллатеральной стороной, что указывает на снижение секреторных возможностей пораженной почки, а также выраженное нарушение показателей выделительной функции почки (рис. 12). Обструктивный тип кривой диагностируется при отсутствии снижения ренографической кривой в течение 20 мин и более после введения радиофармпрепарата. Это происходит при выраженном нарушении функции почки: обструкция конкрементом, выраженная обструкция при патологии мочеточника или сосуда, при выраженных воспалительных изменениях.
Рис. 12. Ренограммы — нарушение показателей выделительной функции почки.
а) Изостенурическая.
б) Обструктивная.
в) Паренхиматозная.
г) Нормальная с незначительным нарушение моторики верхних мочевыделительных путей.
При наличии «маленькой» почки сцинтиграфическое изображение уменьшено в размерах и деформировано; ренографическая кривая изостенурического типа (выраженное снижение или удлинение секреторно-эвакуаторного участка с уплощенным пиком ренограммы) или при нефункционирующей почке афункционального типа (снижение амплитуды сосудистого сегмента), при отсутствии секреторного и экскреторного фрагментов кривой; имеет место выраженное снижение артериального кровоснабжения пораженной почки.
Визуально при динамической ангионефростинтиграфии можно оценить топографию, размеры, форму почек, определить задержку радиофармпрепарата в чашечно-лоханочной системе и мочеточниках (рис. 13).
Рис. 13. Ангионефростингиграфия почек — сцинтиграммы.
а) В норме, на 5-й минуте положение почек типичное, форма сохранена, контуры ровные четкие. Накопление радиофармпрепарата интенсивное, распределение равномерное.
б) При выраженных функциональных нарушениях, на 5-й минуте положение почек типичное, форма сохранена, контуры нечеткие. Накопление радиофармпрепарата интенсивное, распределение диффузно-неравномерное. Отмечается накопление радиофармпрепарата окружающими тканями.
в) В норме, на 19-й минуте определяется накопление РФП в мочевом пузыре. Полное выведение радиофармпрепарата из почек.
г) При выраженных функциональных нарушениях, на 19-й минуте контуры почек нечеткие, распределение радиофармпрепарата неравномерное. Замедление выведения радиофармпрепарата на уровне лоханок, больше справа..
Экскреторная урография позволяет предположить реноваскулярную обструкцию, которая проявляется как симптом Фролея, перегиб в лоханочно-мочеточниковом сегменте, выявить патологию мочеточника: высокое отхождение мочеточника, клапан мочеточника (рис. 14).
Рис. 14. Экскреторные урограммы.
а) Линейный дефект наполнения шейки верхней чашечки правой почки с умеренной эктазией (симптом Фролея), перегиб в лоханочно-мочеточниковом сегменте справа без нарушения оттока (стрелка).
б) Высокое отхождение мочеточника.
в) Клапан мочеточника. Дефект наполнения в начальном отделе мочеточника. Симптом пустого мочеточника Лихтенберга: дилатированная лоханка, отсутствие контраста в мочеточнике.
Начальные признаки, выявляемые на экскреторной урограмме при наличии воспалительных изменений в почках (спастическая стадия пиелонефрита): локальные спазмы чашечно-лоханочной системы, чаще в области верхних чашечек, что соответствует расположению сфинктера Диссе в области шейки малых чашечек; недостаточная контрастность верхних мочевых путей и замедление эвакуации контрастного вещества пораженной почкой вследствие дискинезии чашечно-лоханочной системы (рис. 15 а); пиелоренальный рефлюкс, выявляемый при экскреторной урограмме с компрессией.
Рис. 15. Экскреторные урограммы (25-я минута).
а) Левосторонний пиелонефрит, спастическая стадия. Средние и нижние чашечки левой почки слабо контрастированы, спазмированы, верхняя чашечка умеренно расширена, деформирована.
б) Двухсторонний пиелонефрит, гипотоническая стадия. Двухсторонняя пиелоэктазия, краевой симптом псоаса. Неравномерное контрастирование полостной системы, деформация и нечеткость чашечек правой почки.
Признаки, определяемые на экскреторной урограмме в более поздние сроки воспалительного процесса (гипотоническая стадия пиелонефрита): расширение чашечно-лоханочной системы и мочеточника; краевой симптом псоаса как следствие снижения нервно-мышечного тонуса всей собирательной системы; грибовидная деформация чашечек: сглаженность и атрофия конусов сосочков, закругление форниксов (вследствие отека слизистой, понижения тонуса нервно-мышечного аппарата и развития соединительной ткани); удлинение шеек чашечек, раздвигание чашечек в результате инфильтрации паренхимы (рис. 15 б).
Признаками «маленькой» почки при экскреторной урограмме являются: уменьшение размеров почки, неровность ее контура с множественными втяжениями; сближение чашечек, уменьшение и деформация лоханки в результате склероза, атрофии почечной ткани и почечного синуса; замедление или отсутствие выделения контрастного вещества. В большей степени все эти изменения проявляются при сморщивании почки на фоне воспалительного процесса, в меньшей — при гипоплазии почки, когда функциональная способность «маленькой» почки может быть не нарушена (рис. 16).
Рис. 16. Экскреторная урограмма (15-я минута).
Гипоплазия правой почки — она небольших размеров, чашечки сближены, шейки их укорочены, форниксы деформированы.
Из табл. 2 видно, что наиболее чувствительным методом в выявлении функциональных нарушений даже при минимальных воспалительных изменениях в почках и мочевыводящих путях является динамическая ангионефростинтиграфия. Ранее было показано, что детям было проведено различное сочетание методов лучевой диагностики с целью определения оптимального варианта их комплексного использования. Анализируя сказанное выше, мы считаем, что УЗИ с ЦДК должно быть первичным методом визуализации у детей с патологией почек и мочевыводящих путей. Этот метод обладает рядом достоинств: позволяет оценить положение почек, смещаемость при дыхании, размеры, форму, очертания, дифференцировку кортико-медуллярной системы, ренальный синус с ЧЛС и периренальные ткани.
Таблица 2. Сравнение лучевых методов в диагностике изменений, выявляемых при патологии почек и мочевыводящих путей.
| Метод диагностики | Количество | |
|---|---|---|
| исследований | патологий | |
| Динамическая ангионефросцинтиграфия | 64 | 56 (87,5 %) |
| Экскреторная урография | 113 | 72 (63,7 %) |
| УЗИ с ЦДК | 176 | 105 (59,6 %) |
УЗИ с ЦДК выявляет аномалии количества, положения и структуры почек; диффузные и очаговые изменения паренхимы. Метод высокочувствителен к обструкции мочевых путей. Кроме того, он ориентирует относительно характера заболевания и определяет выбор дальнейшего метода визуализации.
УЗИ с ЦДК имеет преимущества перед экскреторной урографией при выраженном гидронефрозе. Значительная дилатация чашечно-лоханочной системы приводит к сильному «разведению» контрастного вещества и чашечно-лоханочной системы почки на экскреторной урограмме может не контрастироваться, что служит причиной диагноза «нефункционирующая» почка. Проведение УЗИ на аппаратах высокого разрешения с оценкой ренального кровотока позволяет избежать этой ошибки. Сохранение нормальной эхогенности паренхимы даже на фоне ее истончения до 3-4 мм и резкой дилатацией чашечно-лоханочной системы при условии визуализации сосудистого рисунка почки хотя бы только в проекции чашечно-лоханочной системы и медуллярного слоя, и снижение средней скорости кровотока не более чем в 2 раза при сравнении с коллатеральной почкой является прогностически благоприятным .
Однако УЗИ с ЦДК имеет недостатки: не всегда позволяет визуализировать мочеточники, не дает полноценной информации о функции почек. Поэтому рекомендуется после выполнения УЗИ с ЦДК проводить радионуклеидные исследования и(или) экскреторную урограмму в зависимости от клинических показаний, и лишь при необходимости выполнять восходящую цистографию.
Экскреторная урограмма дает обзор всего мочевого тракта, включая мочеточники и мочевой пузырь; позволяет оценить выделительную функцию почек; подтверждает или исключает обструкцию, определяет причины и уровень обструкции.
Сравнивая радионуклеидные методы диагностики и рентгенологические следует сказать, что первые имеют несомненные преимущества перед вторыми. Отсутствие катетеризации мочевого пузыря при непрямой радионуклеидной цистографии позволяет избежать риска инфекции и физиологического дискомфорта у пациентов; при радионуклеидной цистографии для выявления пузырно-мочеточникового рефлюкса не мешают ни костные структуры, ни содержимое кишечника; динамическая ангионефростинтиграфия позволяет не только получить полную информацию о функции мочевыводящей системы, но и оценить количественный вклад пораженной почки в накопительную функцию; радионуклеидные методы диагностики не требуют введения большого объема контрастного вещества и безопасны с точки зрения развития анафилактических реакций; эффективная эквивалетная доза облучения при радионуклеидном исследовании не превышает 0,4 мЗв (независимо от времени и режима записи), при рентгенологическом исследовании составляет 0,8 мЗв и более.
Указанный подход в диагностике и соблюдение строгой последовательности выполнения лучевых методик позволяет диагностировать пузырно-мочеточниковый рефлюкс (УЗИ с ЦДК и непрямая радионуклеидная цистография), оценивать функцию почки (экскреторная урография и динамическая ангионефростинтинтиграфия), определять патологию сосудов (УЗИ с ЦДК), мочеточника и мочевого пузыря (экскреторная урография).
Сочетание УЗИ с ЦДК и восходящей цистографией недостаточно эффективно. Учитывая низкий процент выявления рефлюксов при восходящей цистографии, а также определяемые при выполнении УЗИ с ЦДК различные диффузные и структурные изменения в почках, мы в полной мере не можем определить функцию почек, изменения мочеточника, а следовательно, подтвердить или опровергнуть изменения, выявленные на УЗИ.
Выводы
Сочетанное использование УЗИ с ЦДК и радионуклеидных методов исследования для выявления пузырно-мочеточникового рефлюкса позволяет исключить у многих пациентов восходящую цистографию.
Первым методом визуализации у детей с патологией почек и мочевыводящих путей должно быть УЗИ с ЦДК.
Рентгенологические методы диагностики применять строго по показаниями.
Литература
Доступная эффективность. Универсальный ультразвуковой сканер, компактный дизайн и инновационные возможности.
Пузырно-мочеточниковый рефлюкс (ПМР) представляет собой патологический обратный ток мочи из мочевого пузыря по мочеточнику в почку.
В урологических стационарах примерно у 70% детей с инфекцией мочевых путей при обследовании выявляется пузырно-мочеточниковый рефлюкс.
ПМР все чаще диагностируют у детей с аномалиями мочевой системы, обнаруженными во время УЗИ плода (30%) или после пиелонефрита (20-50%). У детей, не переносивших пиелонефрит, ПМР обнаруживается редко (1%)
Так в каких же случаях можно заподозрить наличие пузырно-мочеточникового рефлюкса:
- Аномалии развития мочевой системы, обнаруженные пренатально (во время беременности при УЗИ плода) и — расширение лоханок и/ или мочеточника выявляемые при проведение ультразвукового исследования почек;
- Частые рецидивирующие инфекции мочевыводящих путей;
Схематическое изображение Пузырно-мочеточникового рефлюкса
«Золотым стандартом» диагностики ПМР является микционная цистоуретерография для определения наличия ПМР и при наличии оценки ее степени. (информацию про данный метод обследования читайте в рубрике методы обследования в урологии). Это исследование должно быть произведено через 2-6 недель после инфекции мочевыводящих путей.
Рентгенологическая картина двусторонней ПМР при проведение микционной цистоуретерографии
В итоге, принимая во внимание степень пузырно мочеточникового рефлюкса и наличие или отсутствие осложнений, подбирают соответственное лечение. Так при 1 степени – лечение консервативное, при 2 и 3 степени – чаще оперативное.
В заключение хотелось бы подчеркнуть, что выбор метода коррекции ПМР должен быть строго индивидуальным и основываться на объективном анализе врачом данных обследования и оценке возможности применения всех имеющихся способов устранения ПМР у данного конкретного больного.
ЛЕЧЕНИЕ ПУЗЫРНО-МОЧЕТОЧНИКОВОГО РЕФЛЮКСА У ДЕТЕЙ В ДОКБ
Пузырно-мочеточниковый рефлюкс (ПМР) является одной из наиболее частых форм нарушения уродинамики в детском возрасте.
У здорового человека моча движется из почки через мочеточник в мочевой пузырь. Если мочевой пузырь полный, давление в нем растет, и клапан пузырного отдела мочеточника смыкается. Поэтому обратное движение мочи исключено. Но при пузырно-мочеточниковом рефлюксе (ПМР) клапан поврежден или ослаблен, и моча движется назад к почке.
Чаще всего такую патологию диагностируют у детей до 2 лет.
Во многих случаях причиной развития рефлюкса у ребенка становится воспаление. В результате него теряется эластичность тканей устья мочеточника, и клапан перестает смыкаться.
Часто ПМР возникает ввиду врожденных аномалий пузырного отдела мочеточника.
Это расстройство уродинамики играет ведущую роль в развитии хронического пиелонефрита, следствием которого является нефрогенная гипертония, а при двустороннем поражении — хроническая почечная недостаточность.
Частота рефлюкса составляет от 0,4 до 1,8 % среди всей популяции, а у детей с инфекцией мочевых путей пузырно-мочеточниковый рефлюкс выявляется у 31,1 %
В связи с этим своевременное лечение ПМР является одной из актуальных проблем.
В норме, мочеточники соединяются с мочевым пузырём таким образом, что образуется клапанный механизм, препятствующий обратному току мочи. В случае различных врождённых патологий, и заболеваний мочевого пузыря, мочеточников, уретры, нервной системы клапанный механизм не формируется или перестаёт действовать. Моча поднимается по мочеточника обратно в лоханку и чашечки почки и даже проникает в ткань почки — паренхиму, что вызывает хроническое воспаление — пиелонефрит и склерозирование паренхимы почки — рефлюкснефропатию.
У кого же из детей можно заподозрить наличие пузырно-мочеточникового рефлюкса. В первую очередь, это дети у которых выявляются изменения в анализах мочи, подъёмы температуры, имеются так называемые дизурические расстройства, т.е. нарушения акта мочеиспускания. Очень часто таким детям первоначально выставляется диагноз: инфекция мочевыводящих путей. Нередко ПМР осложнённый пиелонефритом с начальными проявлениями рефлюкснефропатии маскируется под диагноз: дисметаболическая нефропатия. Это связано с тем, что лабораторный признаки дисметаболической нефропатии, а именно анализ мочи на АКСМ (антикристаллообразующую способность мочи) изменяется в результате поражения клеточных мембран ткани почки на фоне рефлюкснефропатии (что было доказано многочисленными научными исследованиями, в том числе и нашей клиники). Поэтому, все дети с повторяющимися «плохими анализами мочи», нарушением мочеиспускания, требуют тщательного обследования.
Заподозрить наличие ПМР можно данным УЗС, причём достоверность данных возрастает при использовании допплерографии (рис. 1), но наибольшей информативностью обладает рентгенологический метод — микционная цистография (рис.2). При цистографии контрастное вещество по тонкому катетеру, безболезненно вводится в мочевой пузырь и на рентгеновских снимках, выполненных в покое и при мочеиспускании отчётливо определяется проникновение контрастного вещества в мочеточники и в полостную систему почки (чашечно-лоханочную систему). Дальнейший план обследования зависит от выявленной патологии и может включать: лабораторное обследование, экскреторную урография, статическую и динамическую сцинтиграфию почек, уректро-цистоскопию, уродинамическое обследование, консультация невролога.
Для лечения ПМР применяется, как консервативное лечение, направленное на улучшение функции мочевого пузыря и лечение осложнения ПМР — пиелонефрита, так и оперативное лечение для восстановления клапанного механизма в месте впадения мочеточников в мочевой пузырь. Естественно, что план лечения выбирается врачом индивидуально и зависит от выявленных при обследовании пациента причин, вызывающих ПМР и степени ПМР.
Различные методики антирефлюксных операций направлены на удлинение подслизистого туннеля, т.е. увеличение внутрипузырной части мочеточника и изменение угла вхождения мочеточника в мочевой пузырь.
Необходимо отметить, что длительное время основными оперативными методиками лечения ПМР были «открытые» операции по методу Коэна, Политано – Лидбеттера, при которых мочеточник пересаживается в мочевом рузыре на новое место с формированием, так называемого подслизистого туннеля, обеспечивающего клапанный механизм, или применялась операция Грегуара, при которой мочеточник укладывается в разрез стенки мочевого пузыря, без вскрытия его полости. В настоящее время данные операции не потеряли своей актуальности, но основным методом лечения ПМР стала малоинвазивная эндоскопическая коррекция.
Эндоскопический метод заключается в имплантации специальных препаратов в определённые области устья мочеточника, изменяя форму устья и угол вхождения мочеточника в мочевой пузырь (рис. 3). В зависимости от возраста пациента, степени рефлюкса и других индивидуальных особенностей выявляемых при обследовании ребёнка определяются точки имплантации препарата и его состав. Применяются, как рассасывающиеся, так и сохраняющие свой объём вещества. Операция выполняется под кратковременным наркозом, через мочеиспускательный канал с использованием специального, очень тонкого эндоскопа, позволяющего выполнять операцию практически в любом возрасте. При тяжёлом ПМР эндоскопическое вмешательство может потребовать повторения, в редких случаях применения открытой операции.
Урологическое отделение ДОКБ оснащено всей необходимой эндоскопической аппаратурой фирмы KARL STORZ (Германия) (рис. 4), врачи отделения имеют большой опыт в проведении эндоскопических операций по коррекции пузырно — мочеточникового рефлюкса.
При эндоскопической коррекции ПМР отсутствует длительный и тяжелый для ребенка послеоперационный период с необходимость массивной антибактериальной терапии. Дети легко переносят операцию без разрезов и быстро выписываются из стационара.
Главное вовремя заподозрить заболевание и выполнить необходимое полноценное обследование. В дальнейшем дети перенесшие коррекцию ПМР наблюдаются урологом, проходят курсы лечения в целях профилактики осложнений перенесённого ПМР, предотвращения склеротических изменений в почечной паренхиме.
Врач уролог — андролог
урологического отделения
ДОКБ к.м.н. А.Л. Аврасин
