Несмотря на то, что эндометриоз был описан еще в XIX в., полностью причины его появления и распространения не изучены. Также многие вопросы относительно методов лечения остаются далекими от решения. В связи с хроническим и часто рецидивирующим характером течения заболевания Комитет врачебной практики Американского общества репродуктивной медицины (ASRM) заключил следующее: «эндометриоз должен рассматриваться как хроническое заболевание, требующее пожизненного плана ведения, приоритетом которого является медикаментозное лечение и профилактика повторных хирургических процедур» .
План лечения должен быть индивидуальным в зависимости от симптомов эндометриоза, распространенности патологического процесса, желания иметь детей, возраста, опыта хирурга, побочных эффектов препаратов и хирургического лечения и т. д. Возможные методы лечения следующие:
- симптоматическое лечение нестероидными противовоспалительными препаратами (НПВП);
- гормональное лечение (комбинированные оральные контрацептивы (КОК) в циклическом или пролонгированном режиме, агонисты гонадотропин-рилизинг-гормонов (ГнРГ), даназол, ингибиторы ароматазы);
- хирургическое лечение, которое разделяют на консервативное (органосохраняющее), т. е. с сохранением матки и ткани яичников, и радикальное: с удалением матки и, возможно, яичников;
- комплексное лечение: сочетание медикаментозного лечения до и/или после хирургии.
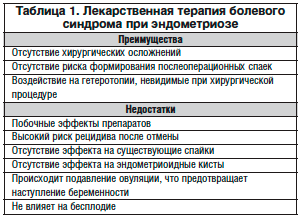
Лапароскопия, бесспорно, является «золотым стандартом» в диагностике и лечении эндометриоза, позволяет коагулировать или иссекать гетеротопии и спайки, и таким образом если не предотвратить, то, как минимум, значительно отсрочить рецидив болезни. Также полное удаление очагов позволяет снизить расходы и побочные реакции медикаментозной терапии. В то же время нередки интраоперационные осложнения, связанные с повреждением нижних отделов кишечника и мочеполового тракта, инфекционные осложнения и формирование послеоперационных спаек, иногда более выраженных, чем до операции. Преимущества и недостатки медикаментозной терапии приведены в таблице 1.
НПВП часто применяются женщинами для купирования болевого синдрома, однако клинические исследования крайне скудны. Главным сдерживающим фактором длительного использования НПВП являются побочные эффекты, такие как язва желудка и ановуляторный эффект при применении в середине менструального цикла .
Наиболее часто в клинической практике для лечения эндометриоза используются агонисты ГнРГ, даназол и некоторые прогестины. Эти препараты и КОК имеют общее воздействие на эндометриоз. По сравнению с эутопическим эндометрием эндометрий в имплантатах синтезирует больше простагландинов, эстрогенов и провоспалительных цитокинов, это приводит к пролиферации и инфильтративному росту, обусловливая боль. Более того, повышенная активность ароматазы потенцирует синтез циклооксигеназы 2-го типа и выработки простагландина Е2, который усиливает синтез эстрогенов. Таким образом, любой препарат, снижающий синтез эстрогенов в яичниках, негативно влияет на этот патогенетический механизм и снижает эндометриоз-ассоциированную боль.
КОК широко применяются для лечения симптомов эндометриоза, однако, судя по данным исследований, эффект незначительный. P. Verchellini et al. полагают, что действие препаратов заключается в подавлении имплантации гетеротопий, но имеется и протективный эффект против их некроза . В состав большинства КОК входит этинилэстрадиол, значительно более активный, чем эстрадиол. В настоящее время высказываются опасения, что этинилэстрадиол может поддерживать локальную гиперэстрогению в гетеротопиях, таким образом «подстегивая» эндометрий. Хотя КОК не входят в протоколы лечения эндометриоза во многих странах, тем не менее, их используют долгое время при необходимости в контрацепции у таких больных. Главная проблема — прорывные кровотечения, которые могут прекратиться при отмене препарата, и через несколько дней можно возобновить лечение. Также КОК не имеют зарегистрированных показаний для лечения эндометриоза, хотя и указаны во многих национальных руководствах и стандартах лечения.
Возможно применение непероральных эстрогенпрогестероновых контрацептивов, однако этот вопрос изучен недостаточно.
Даназол — это андрогенный стероидный препарат, достаточно эффективный при лечении эндометриоза. По данным исследований, более 80% пациенток отмечают исчезновение или значительное ослабление боли , но его применение ограничено частыми побочными эффектами: влиянием на липидный профиль, прибавкой массы тела, отечностью, усилением секреции сальных желез и акне, сухостью во влагалище, приливами, гирсутизмом, гепатотоксичностью и атрофией молочных желез.
Пероральные, парентеральные, внутриматочные контрацептивы или прогестины в виде имплантатов используются в течение десятилетий с различной доказательной базой. Однако для достижения терапевтического эффекта зачастую необходимо переходить на более высокие дозировки по сравнению с другими показаниями для их применения, что, конечно, увеличивает частоту побочных реакций (прибавка массы тела, андрогенные эффекты и сердечно-сосудистые осложнения) .
Отдельного внимания заслуживает препарат диеногест (Визанна, Bayer, Германия), который рекомендован в качестве монотерапии эндометриоза в Европе, Японии и др. Он представляет собой синтетический пероральный прогестин с выраженным прогестагенным и умеренным антигонадотропным эффектами, но без андрогенной, глюкокортикоидной и минералокортикоидной активности. Механизм действия на эндометриоидные гетеротопии многофакторный. Диеногест снижает секрецию гонадотропинов, что приводит к значительному снижению синтеза эстрадиола. При продолжительном применении вызывает гипоэстрогению, повышение уровня прогестерона, что приводит к децидуализации, а затем атрофии эндометриальной ткани . В эксперименте на животных также показано, что диеногест вызывает апоптоз гранулезных клеток яичников . В исследованиях на животных показано следующее влияние диеногеста: подавление пролиферации, ангиогенеза и противовоспалительный эффект диеногеста .
Рандомизированное клиническое исследование показало, что перорально принимаемый диеногест более эффективен по сравнению с плацебо, уменьшая боль при подтвержденном эндометриозе . В исследованиях, сравнивающих прием диеногеста длительностью 16 и 24 нед. вместе с агонистами ГнРГ у пациентов с эндометриозом, и прием агонистов ГнРГ, получены сопоставимые результаты по уменьшению боли по баллам и по классификации эндометриоза rAFS при повторной лапароскопии . Другое рандомизированное исследование, сравнивающее агонисты ГнРГ и диеногест, предлагают последний как сопоставимый по эффективности, но более безопасный и лучше переносимый, что связано с меньшей гипоэстрогенией, меньшими изменениями минеральной плотности костной ткани и маркеров костной резорбции .
Общеизвестно, что самые эффективные методы снижения продукции эстрогенов — это двухсторонняя овариоэктомия и применение агонистов ГнРГ. По понятным причинам удаление яичников в репродуктивном возрасте выполняется крайне редко. Однако частое и длительное применение агонистов ГнРГ ограничено в связи с высокой ценой и побочными эффектами, обусловленными гипоэстрогенией (аменорея, вазомоторные симптомы (80%), нарушение сна, приливы, урогенитальная атрофия (30%), головные боли (30%) и снижение минеральной плотности костной ткани (МПКТ); доказано, что применение ГнРГ увеличивает риск переломов спустя годы после приема препаратов. В 48-недельном рандомизированном исследовании показано, что при лечении агонистами ГнРГ в длительном режиме в сочетании с другими препаратами (add-back-терапия) качество жизни и эффективность сопоставимы с таковыми при применении КОК в непрерывном режиме .
Для выяснения оптимального длительного режима add-back-терапии проведено одно большое рандомизированное плацебо-контролируемое исследование. Пациентки с эндометриоз-ассоциированной болью распределены на 4 группы:
- Агонисты ГнРГ в дозе 3,75 мг в/м каждые 4 нед.
- Агонисты ГнРГ и прогестин (норэтиндрона ацетат 5 мг 1 р./сут).
- Агонисты ГнРГ и малые дозы конъюгированного эстрогена 0,625 мг и прогестин (норэтиндрона ацетат 5 мг 1 р./сут).
- Агонисты ГнРГ и конъюгированный эстроген в высокой дозе (1,25 мг 1 р./сут) и прогестин (норэтиндрона ацетат 5 мг 1 р./сут).
Всем пациенткам назначался кальций 1000 мг/сут на весь срок лечения . В результате данного исследования выяснилось, что женщины без add-back-терапии или с прогестином с добавлением 0,625 мг эстрогена или без него имели одинаковые показатели снижения тазовой боли. Добавление низких доз эстрогенов было более эффективно, чем высоких (1,25 мг). В группе с высокой дозой эстрогенов пациентки чаще прекращали лечение из-за боли, вероятно, в связи с тем, что это достаточная доза для поддержания роста и функционирования гетеротопий, что подтверждается и другими исследованиями . МПКТ значимо снижается только в группе без add-back-терапии, в остальных группах различий в минеральной плотности костной ткани до и после лечения выявлено не было. Вазомоторные симптомы были значительно снижены во всех группах с add-back-терапией. При отслеживании этих пациентов через 12 и 24 мес. после окончания лечения во всех группах симптомы были менее выраженные, чем через 8 мес. после начала активной терапии . В случае, когда невозможно проводить add-back-терапию стероидными препаратами, разработаны схемы снижения доз агонистов ГнРГ или увеличения интервала приема.
Следует отметить, что на момент написания статьи препарат диеногест еще не зарегистрирован в США, что связано с правилами регистрации в стране. Первой линией терапии являются агонисты ГнРГ и прогестины (уровень доказательности IА). При непереносимости побочных эффектов применения высоких доз некоторых прогестинов предполагается использовать агонисты ГнРГ и низкие дозы эстрогенов и прогестина (уровень доказательности IIА).
Конечно, оптимальный режим add-back-терапии еще предстоит выяснить, более того, нет сравнительных исследований препарата диеногест с агонистами ГнРГ в сочетании с поддерживающей терапией. Однако, возможно, в будущем в схемах лечения эндометриоза будет сочетание диеногеста и агонистов ГнРГ или их последовательное применение. В пользу этого говорит одно нерандомизированное исследование из Японии, сравнивающее применение диеногеста в дозе 2 мг/сут 12 мес. с последовательным лечением агонистами ГнРГ 4–6 мес., после чего назначался диеногест 1 мг/сут . Были получены обнадеживающие результаты; авторы заключают, что длительное применение диеногеста у женщин после лечения агонистами ГнРГ является обоснованным.
Необходимо признать, что в выборе терапии немаловажным фактором является стоимость, т. к. все расходы фактически ложатся на плечи женщины. Любая длительная схема, включающая в себя агонисты ГнРГ, очень затратна и должна быть обоснована с позиции эффективности и безопасности. В этом плане выгодно отличается диеногест, побочные эффекты которого предсказуемы. Однако выраженный клинический эффект не позволяет пациенткам отказываться от лечения в подавляющем большинстве случаев. Тем не менее необходимы более масштабные исследования, направленные на оценку экономической целесообразности применения диеногеста.
Применение ингибиторов ароматазы — это новый многообещающий метод лечения эндометриоза. Эти препараты снижают локальный синтез эстрогенов в эндометриоидных гетеротопиях, к тому же ингибируют образование эстрогенов в яичниках, головном мозге и жировой ткани . В эндометриоидных очагах простагландин E2 стимулирует гиперпродукцию ароматазы, что приводит к локальному синтезу эстрогенов из андрогенов. Эстрогены в свою очередь увеличивают синтез простагландина E2, обеспечивая положительную обратную связь. В нескольких описательных работах и одном рандомизированном исследовании ингибиторы ароматазы использовались для лечения тяжелых форм эндометриоза . При систематическом обзоре этих исследований выяснилось, что ингибиторы ароматазы статистически значимо более выраженно снижают боль в сравнении с агонистами ГнРГ . Важно знать, что ингибиторы ароматазы вызывают значительную потерю костной плотности при длительном применении и не могут назначаться в виде монотерапии у пременопаузальных женщин, т. к. вызывают мультифолликулярные изменения в яичниках за счет стимуляции ФСГ. В этом случае целесообразно сочетание с агонистами ГнРГ или эстроген-прогестиновыми контрацептивами .
Еще одним перспективным направлением в лечении эндометриоза является попытка минимизировать воспалительный компонент в гетеротопиях. Важная роль в генезе симптомов эндометриоза отводится провоспалительным цитокинам и активации оксидативного стресса, при этом происходит активация внутриядерного воспалительного медиатора NF-B (ядерный фактор каппа-энхансер легких цепей активированных B-клеток), который может поддерживать воспалительный ответ и стимулировать ангиогенез. Однако систематические обзоры не доказали целесообразность применения антагонистов TNF-α или пентоксифиллина для лечения симптомного эндометриоза.
В качестве заключения хочется отметить общую мысль, проходящую через многие обзорные статьи. В частности, в статье P. Vercellini из Миланского университета с символическим названием «В ожидании Годо» авторы достаточно скептически и пессимистично относятся к современным фармакологическим методам лечения эндометриоза. Делается вывод о том, что многие женщины за свою жизнь, несмотря на применение современных и дорогостоящих препаратов, не избегут повторных операций, таким образом, «должны ли мы все еще ждать Годо»?
Литература
Сильные боли внизу живота (такие, что вести привычный образ жизни невозможно), нарушение менструальной функции могут сигнализировать о развитии эндометриоза. В примерно 50% случаев эта болезнь становится причиной бесплодия. В 85-90% сочетается с миомой матки.
Содержание
- Что такое эндометриоз?
- Почему возникает эндометриоз?
- Как диагностируют эндометриоз?
- Последствия эндометриоза
- Лечение эндометриоза
- Миф №1: Эндометриоз встречается редко
- Миф №2: Менструация должна быть болезненной
- Миф №3: Эндометриоз не развивается у подростков и молодых женщин в возрасте до 20-ти лет
- Миф №4: Для постановки диагноза «эндометриоз» должны присутствовать все симптомы, характерные для данного заболевания
- Миф №5: Врач может диагностировать эндометриоз даже после первичной беседы и описания симптомов женщиной
- Миф №6: Эндометриоз является легким заболеванием, которое не имеет долгосрочных последствий
- Миф №7: Беременность может вылечить эндометриоз
- Миф №8: Менопауза лечит эндометриоз
- Миф №9: Эндометриоз – это чрезмерное разрастание эндометрия в матке
- Миф №10: Эндометриоз является заболеванием амбициозных женщин
- Миф №11: Гистерэктомия – это метод лечения эндометриоза
- Миф №12: С диагнозом эндометриоз хирургическое вмешательство должно осуществляться через большой разрез брюшной полости, чтобы хирург смог все увидеть
- Миф №13: овариэктомия (удаление яичника) лечит эндометриоз
- Миф №14. Гормональные препараты способны вылечить эндометриоз
- Миф №15. Удаление очагов эндометриоза вместе с гистерэктомией или отдельно от нее является единственным путем лечения данного заболевания
- Миф №16: резекция кишечника всегда необходима для лечения эндометриоза кишечника
Что такое эндометриоз?
Эндометриоз – хроническое гормонозависимое заболевание, при котором очаги эндометрия (внутреннего слоя матки) появляются за пределами нормального расположения (в яичниках, маточных трубах, брюшной полости. Бывает также эндометриоз глаз, костей, суставов, послеоперационного рубца и др.).
Почему возникает эндометриоз?
Общие рекомендации врачей-акушеров-гинекологов: воздерживаться в период менструации от половой жизни и от любых манипуляций (физиопроцедур, медисследований, операций и др.). В это время их проведение увеличивают риск развития заболевания. Хирургическое вмешательство на органах малого таза, брюшной полости также провоцирует развитие эндометриоза.
Как диагностируют эндометриоз?
- Жалобы пациенток. Чаще всего эндометриоз проявляется сильными болями внизу живота, нарушением менструальной функции, иногда кровотечениями. Почти всегда в одной связке с этой патологией идет миома матки. Но иногда эндометриоз может протекать бессимптомно и его обнаружение может стать случайной находкой.
- Пальпаторно. Опытный врач может нащупать новообразования в матке и яичниках на осмотре.
- УЗИ. Современный и безболезненный метод диагностики. УЗИ-аппараты экспертного класса медицинского центра «МедАвеню» позволяют не просто обнаружить образование, но и определить толщину эндометрия, оценить наличие взвесей, вязкости эндометрия, что станет хорошим подспорьем для более точной диагностики патологии.
- Гистероскопия. Метод, при котором в полость матки вводят видеокамеру.
- Кольпоскопия. Это способ осмотреть шейку матки и влагалище при помощи специального «микроскопа».
- Лапароскопия. Считается «золотым стандартом» в диагностике эндометриоза. Это миниинвазивная (с помощью небольших проколов) хирургическая операция, которая позволяет заглянуть в брюшную полость. Выполняется в условиях стационара.
Татьяна Смирнова, врач-акушер-гинеколог высшей категории медицинского центра «МедАвеню», доцент кафедры акушерства и гинекологии Белгосмедуниверситета, кандидат меднаук; врачебный стаж — 36 лет:
«В диагностике никогда нельзя использовать только какой-то один метод. Их обязательно должно применяться несколько. И все это работает в совокупности с клиническим мышлением врача, с его уровнем подготовки. Чем раньше и точнее поставлен диагноз, тем быстрее начато лечение. И тем выше его эффективность. В том числе мы можем уберечь наших пациенток от хирургического лечения».
Последствия эндометриоза
Если эндометриоз не лечить, его очаги разрастаются. Впоследствии это может приводить к необходимости удалить яичники и матку.
Татьяна Смирнова, врач-акушер-гинеколог высшей категории медицинского центра «МедАвеню», доцент кафедры акушерства и гинекологии Белгосмедуниверситета, кандидат меднаук; врачебный стаж — 36 лет:
«Матка — орган, который требует к себе уважения. Это не просто плодовместилище. При удалении матки прекращается выработка простогландинов в организме женщины. А эти физиологически активные вещества способствуют профилактике инсультов и инфарктов. Поэтому после такой операции возрастает их риск».
Лечение эндометриоза
Главным методом лечения эндометриоза все еще остается хирургический: очаги болезни удаляют при помощи лапароскопической операции. Но в данном случае есть большой риск того, что эндометриоз вернется. К тому же, при хирургическом вмешательстве на яичниках уменьшается их овариальный резерв (генетически заложенное количество фолликулов для хранения яйцеклеток). Это влияет на способность молодых женщин становиться мамами.
К счастью, современная медицина ратует за избавление от патологий «без скальпеля». Для гинекологических заболеваний, в том числе эндометриоза и миомы матки, в медицинском центре «МедАвеню» успешно применяется консервативная терапия — прогестагены (диеногест) и агонисты гонадотропин-рилизинг гормона. Она рекомендуется при эндометриоидных кистах малого размера (до 3 см) и болевом синдроме.
Как часто обращаться к гинекологу?
При наличии жалоб, выявленных проблем (эндометриоз, миома матки и другие) — не реже одного раза в 3 месяца. Если вас ничего не беспокоит, профилактический осмотр у врача-акушера-гинеколога рекомендуется раз в год.
Эндометриоз – сложное и неоднозначное заболевание, вокруг которого существует большое количество мифов и заблуждений. Не одно поколение медиков ломает голову над решением диагностических и лечебных вопросов, связанных с ним. Попробуем прояснить наиболее распространенные мифы, которые кружат вокруг диагноза «Эндометриоз».
Миф №1: Эндометриоз встречается редко
Факты: Эндометриоз является одним из самых распространенных гинекологических заболеваний.
Трудно оценить, сколько именно женщин страдают эндометриозом, потому что большинство из них не имеет каких-либо заметных симптомов. Одной из основных жалоб может быть только боль, особенно во время менструации. Сотрудники здравоохранения подсчитали, что около 40-60% женщин, имеющих очень болезненные месячные, страдают эндометриозом.
Миф №2: Менструация должна быть болезненной
Факты: Одним из симптомов эндометриоза является интенсивная тазовая боль, ее сила оценивается от 6 до 10 баллов.
Мифы вокруг менструации существовали с незапамятных времен. Люди раньше верили, что зубы женщины во время менструации не должны быть запломбированными, так как пломбы все равно будут в это время выпадать. Среди таких же верований находится и утверждение о том, что менструация должна быть болезненной. Вы должны следить за своим телом тщательно. Если менструальная боль не позволяет шагать в обычном ритме повседневной жизни, то это может быть первым и единственным симптомом такого заболевания, как эндометриоз.
Миф №3: Эндометриоз не развивается у подростков и молодых женщин в возрасте до 20-ти лет
Факты: Эндометриоз может не проявляться у женщины до того момента, пока она не захочет иметь ребенка, и не возникнет проблема бесплодия.
Миф, что эндометриоз поражает только женщин в зрелом возрасте, до сих пор сохраняется в нашем обществе. Многие подростки и молодые женщины, которые могут страдать от эндометриоза, не обращаются к гинекологу, так как считают, что болезненные месячные – это вариант нормы. По данным литературы, более 2/3 женщин с эндометриозом страдают от симптомов еще до достижения ими 20-летнего возраста. 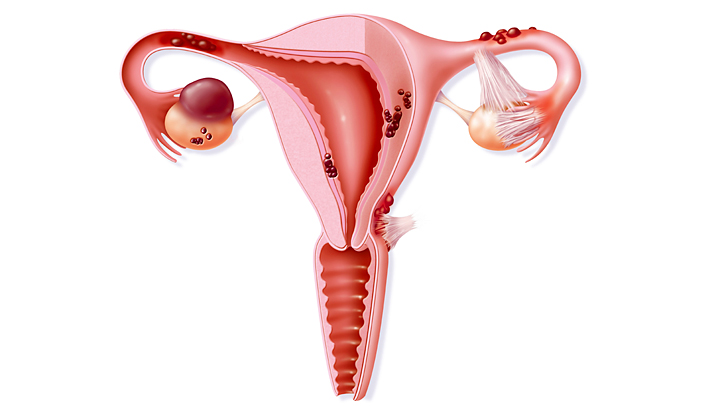 Эндометриоз
Эндометриоз
Миф №4: Для постановки диагноза «эндометриоз» должны присутствовать все симптомы, характерные для данного заболевания
Факты: к признакам эндометриоза относятся болезненные месячные, боли в области малого таза, овуляторные боли, боли при половых сношениях, значительные или нерегулярные менструальные кровотечения, тяжесть и боль во время актов дефекации или мочеиспускания, особенно во время менструации.
Некоторые женщины с эндометриозом могут не отмечать ни одной из этих жалоб, некоторые будут иметь только одну жалобу, а другие будут жаловаться на более чем один из перечисленных симптомов. Каждая женщина уникальна в том, как эти симптомы могут или не могут проявляться. Верно также и то, что тяжесть или степень распространения эндометриоза не всегда связана с тяжестью симптомов, которые беспокоят.
Миф №5: Врач может диагностировать эндометриоз даже после первичной беседы и описания симптомов женщиной
Факты: Ваш врач или гинеколог обязательно должен учитывать историю появления всех симптомов, когда речь идет о постановке диагноза.
Но, как правило, только УЗИ и лапароскопия смогут подтвердить окончательный диагноз. Лапароскопия – это минимально инвазивное хирургическое вмешательство (часто называют «пупок» -операция), так как через пупок в живот вводится лапароскоп с видеокамерой, чтобы посмотреть на ваши половые органы. Во время лапароскопии визуализируются все очаги эндометриоза, а также есть возможность удаления этих очагов, что является одним из лечебных шагов. В течение нескольких месяцев после лапароскопии женщины могут забеременеть самостоятельно. Однако это не является обязательным и типичным для всех.
Миф №6: Эндометриоз является легким заболеванием, которое не имеет долгосрочных последствий
Факты: В то время как молодые женщины практически могут не чувствовать никаких симптомов, связанных с эндометриозом, у женщин пожилого возраста проявления заболевания будут зависеть от степени его распространения и влиять на все аспекты жизни женщины.
Боль при эндометриозе может повлиять на способность человека работать, выполнять повседневные дела по дому или иметь сексуальные отношения. Некоторые женщины годами терпят боль и дискомфорт, что в конечном итоге может привести к тотальной гистерэктомии. Эндометриоз также может значительно ухудшить способность к оплодотворению. Известно, что около 30-40% женщин с эндометриозом имеют проблемы с фертильностью. Эндометриоз считается одной из трех главных причин женского бесплодия. 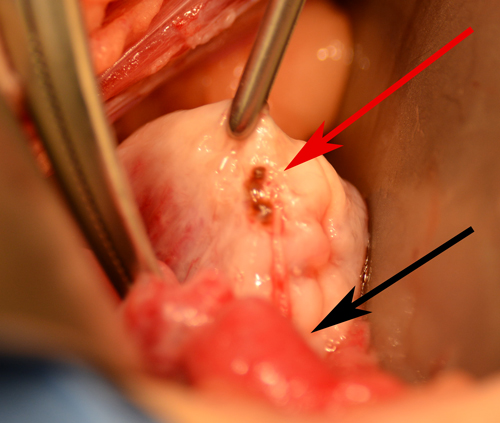 Красная стрелка указывает на очаг эндометриоза в яичнике, черная – на фаллопиеву трубу
Красная стрелка указывает на очаг эндометриоза в яичнике, черная – на фаллопиеву трубу
Миф №7: Беременность может вылечить эндометриоз
Беременность считается состоянием природной гормональной терапии, при которой большинство проявлений эндометриоза может исчезнуть. К сожалению, из-за высокого уровня эстрогена, особенно в первые два триместра, симптомы могут стать еще более выраженными. И все жалобы возобновятся с возвращением первой менструации.
Миф родился в пятидесятые годы, когда было зафиксировано, что эндометриоз у родивших женщин был менее выраженным, чем у тех, кто не рожал. К сожалению, со временем оказалось, что причина и следствие смешались – а связано это все с тем, что у женщин с менее выраженными проявлениями эндометриоза беременность наступила самостоятельно.
Миф №8: Менопауза лечит эндометриоз
Несмотря на неприятные ощущения, сопровождающие период менопаузы, многие из женщин, страдающих от эндометриоза, с нетерпением ждут наступления этого периода. Во время менопаузы организм перестает вырабатывать эстроген – гормон, отвечающий за рост эндометрия матки. Так, обильные кровотечения останавливаются, но не сам эндометриоз. Женщины, которые находятся на гормональной заместительной терапии, или те, чей организм продолжает вырабатывать маленькое количество эстрогена, например женщины с ожирением, могут по-прежнему страдать от дискомфортных ощущений, связанных с присутствием очагов эндометриоза.
Миф №9: Эндометриоз – это чрезмерное разрастание эндометрия в матке
Чрезмерный рост эндометрия, чрезмерное утолщение слизистой оболочки матки связаны с гормональными нарушениями. Следствием этого является сильное кровотечение. Разрастание эндометрия может быть диагностировано с помощью трансвагинального УЗИ.
Эндометриоз, с другой стороны, приводит к наличию очагов «внутренней слизистой оболочки» матки (эндометрия) вне полости матки. Это может быть диагностировано с помощью лапароскопии.
Это означает, что рост собственно эндометрия и появление эндометриоидных очагов являются самостоятельными элементами заболевания.
Миф №10: Эндометриоз является заболеванием амбициозных женщин
Этот миф родился полвека назад. Исследования, проведенные в 1950-1970 гг., показали, что симптомы, характерные для эндометриоза, чаще встречаются у женщин, которые откладывают свое решение относительно наступления беременности. Как правило – это дамы, которые не были заинтересованы в создании семьи, так называемые «карьеристки», для которых работа была важнее, чем семья. Вот почему эндометриоз долгое время считался «болезнью амбициозных женщин». Исследование, которое прошло за последние десятки лет, показало, что эта теория ошибочна, и нет никакой связи между болезнью и амбициями. Причины заболевания гораздо сложнее.
Миф №11: Гистерэктомия – это метод лечения эндометриоза
Факт: гистерэктомия не является панацеей для эндометриоза.
Эндометриоз – это состояние, которое существует за пределами матки, поэтому удаление матки не решает вопрос, и эндометриоз может достаточно долго и хорошо существовать без матки. Это только теория, что эндометриоз начинается с эндометрия, поэтому удаление матки не может предотвратить образование новых очагов эндометриоза. Таким образом, удаление матки не лечит эндометриоз.
Миф №12: С диагнозом эндометриоз хирургическое вмешательство должно осуществляться через большой разрез брюшной полости, чтобы хирург смог все увидеть
Факт: Хирургия для лечения эндометриоза может проводиться с помощью лапароскопических и других минимально инвазивных методов.
Многие специалисты по эндометриозу являются опытными специалистами в области минимально инвазивной хирургии. Кроме того, некоторые из инструментов, используемых при эндоскопических методиках, дают возможность многократного увеличения, что значительно повышает видимость очагов при одновременной минимизации рисков, которые являются при открытых абдоминальных хирургических вмешательствах.
Миф №13: овариэктомия (удаление яичника) лечит эндометриоз
Факт: Удаление яичников не лечит эндометриоз.
Хотя и основой эндометриоза является влияние эстрогенов, которые в большом количестве вырабатываются в яичниках, но отсутствие яичника не означает, что у женщины не будет эндометриоза. Есть много других путей попадания эстрогенов в организм женщины без участия яичников. Присутствие любых очагов эндометриоза – это основа для дальнейшего развития данного заболевания, даже при удаленном яичнике. Таким образом, удаление яичников не является обязательным для эндометриоза, так как лечит его.
Миф №14. Гормональные препараты способны вылечить эндометриоз
На протяжении многих лет для лечения эндометриоза применяются синтетические гормональные препараты. Однако недавние исследования показали, что эти препараты не обладают длительным эффектом. Эти гормоны просто подавляют проявления эндометриоза, но только на то время, пока больная их принимает. Как только прием препаратов прекращается, симптомы заболевания появляются вновь.
Миф №15. Удаление очагов эндометриоза вместе с гистерэктомией или отдельно от нее является единственным путем лечения данного заболевания
Факт: Удаление может быть успешным вариантом лечения для эндометриоза, но оно не может быть полным и единственным методом. Есть и другие варианты лечения, которые могут быть успешно использованы.
Есть достаточно противоречивые факты относительно окончательных методов лечения эндометриоза. Некоторые специалисты по эндометриозу считают, что удаление эндометриоидных очагов является единственным методом лечения, в то время как другие специалисты утверждают, что нет окончательного лечения, даже после успешного удаления очагов есть пациенты с рецидивами. Результат может также зависеть от типа пациентов и стадии заболевания.
Цель операции – найти и удалить как можно больше эндометриоидных очагов. Хотя и удаление может быть довольно успешным, сочетание методов считается достаточно целесообразным, чтобы устранить все возможные гетеротопии, даже те, которые не удалось визуализировать. Ключ к хирургическому лечению эндометриоза – это квалифицированный и специализированный хирург, который способен успешно использовать различные методики.
Миф №16: резекция кишечника всегда необходима для лечения эндометриоза кишечника
Факт: В некоторых случаях, эндометриоз может быть удален из кишечника без необходимости резекции.
Если эндометриоз не проникает сквозь слои кишечника, его могут вырезать из стенки, не проводя резекцию. Это может свести к минимуму как риски и осложнения, так и реабилитацию в послеоперационном периоде.
Суть в том, что только Вы знаете ваше тело. Если Вы чувствуете, что что-то отличается от вашего обычного беззаботного самочувствия, появились какие-то дискомфортные ощущения, беспокоит боль во время половых актов или менструальные боли, тяжелые или нерегулярные менструальные кровотечения, или есть проблемы с зачатием, то пришло время обратиться к гинекологу. Не игнорируйте свои чувства и не ждите, пока они станут более интенсивными, обращайтесь за медицинской помощью вовремя.
Чтобы помочь Вам определить, какое именно лечение медикаментозное или хирургическое является правильным для Вас и Вашего диагноза «ЭНДОМЕТРИОЗ», Вам необходимо найти именно тех специалистов, которые специализируются на проблеме эндометриоза. Их хирургический опыт и обучение могут быть весьма полезными в проведении лечения эндометриоза, учитывая сложность и неоднозначность заболевания.
Анна Новосад, врач-гинеколог Центра здоровья женщины Универсальной клиники «Оберіг»
Эндометриоз — это гормонозависимое хроническое воспалительное гинекологическое заболевание, вызывающее симптомы тазовой боли, влияющие на физическое, психическое и социальное благополучие женщин репродуктивного возраста .
Несмотря на высокую распространенность, которая по оценкам составляет от 6% до 10% , и признанное экономическое бремя, связанное с этим заболеванием , его этиология остается во многом еще не изученной. Роль питания в определении становления и прогрессирования эндометриоза в последнее время стала предметом интереса, главным образом из-за наблюдения, что некоторые физиологические и патологические процессы, связанные с этим заболеванием, такие как воспаление, активность эстрогенов, менструальная цикличность, хлорорганическая нагрузка и метаболизм простагландинов, могут быть подвержены влиянию диеты .
Зависимость заболевания от эстрогенов особенно актуальна в этом контексте. В других условиях, в которых гормоны играют специфическую роль, таких как молочные железы и рак эндометрия , научные исследования показали, что диета и избыток жиров могут сильно влиять на заболеваемость. Специфические привычные диетические схемы, по-видимому, оказывают умеренное влияние на некоторые маркеры воспаления, которые, как было показано, увеличиваются при эндометриозе :
1) полихлорированные дифенилы, которые склонны к биоаккумуляции, в частности в липидах (мясо, печень и молочные продукты) ;
2) пестициды/инсектициды, которые могут поступать в организм через потребление загрязненных овощей и фруктов , — было предложено в качестве факторов риска развития эндометриоза с начала 1990-х годов .
На этих основаниях литература о роли диеты в риске эндометриоза систематически пересматривается, оценивая как питательные вещества, так и группы продуктов питания, с целью выявления потенциальных модифицируемых факторов риска заболевания.
В электронных базах данных MEDLINE (с 1966 по 2018 г.), EMBASE (1985 по 2018 г.) и Science Citation Index Expanded (с 1945 по 2018 г.) осуществлялся поиск по медицинским рубрикам терминов «диета», «питание», «витамины», «жиры», «овощи», «кофе», «кофеин», «мясо», «рыба», «молочные продукты» или «фрукты» в сочетании с «эндометриозом». Рассматривались только те публикации, которые были опубликованы в виде полнометражных статей и на английском языке. При наличии нескольких опубликованных отчетов по одному и тому же исследованию включался только тот, в котором содержалась наиболее подробная информация. Обзорные статьи рассматривались только в том случае, если были представлены и оригинальные данные. Тезисы докладов научных совещаний не включались. Для каждого исследования была извлечена следующая информация: фамилия первого автора; год публикации; cтрана происхождения; количество субъектов и случаев; дизайн исследования; категория количества потребляемых питательных веществ. Информация о потенциальной роли рассматриваемых питательных веществ была представлена в соответствии с тем способом, в котором результаты были представлены в оригинальных работах. Учитывая скудость представленной до сих пор информации, результаты, полученные при потреблении конкретных продуктов питания, иногда описывались и обсуждались вместе с теми, кто сообщал об основных питательных веществах, содержащихся в них (например, красное мясо и насыщенные жиры). Объединенная оценка не рассматривалась, поскольку клиническая (исследуемые популяции), методологическая (частотная классификация воздействия) и статистическая (корректировка на смешивающие факторы) неоднородности присутствуют во всех исследованиях. Поэтому, чтобы избежать ошибочных выводов, результаты этого систематического обзора представлены с использованием более качественного подхода.
Информация о потреблении пищи была собрана с помощью опросников по выявлению частоты потребления продуктов питания в семи исследованиях, в то время как в одном исследовании опросник был сосредоточен на потреблении кофеина и алкоголя. Простые вопросы «нет» или «да» использовались в одном исследовании для оценки потребления кофе . Следует учитывать, что выявленные исследования характеризуются выраженными различиями в категоризации экспозиции, аналитических подходах, фенотипах заболеваний, рассматриваемых питательных веществах и общем методическом оформлении. Все эти аспекты следует учитывать при интерпретации противоречивых результатов, полученных в ходе различных исследований. Дизайн исследования, представленные результаты основаны на исследованиях «случай-контроль». Было выявлено только одно когортное проспективное исследование . Ретроспективный сбор продуктов питания затруднен, особенно при длительно протекающих заболеваниях. Женщины с эндометриозом обычно испытывают 6–10-летнюю задержку между появлением симптомов и окончательным диагнозом, и болезнь может прогрессировать . Они могли изменить свои диетические привычки в начале заболевания, или их диета могла повлиять на болевые ощущения, лежащие в основе заболевания и требующие постановки диагноза.
Диетическая информация собиралась различными методами в различных исследованиях, поэтому трудно сравнивать результаты различных исследований. Кроме того, различная структура питания в различных странах является хорошо известной проблемой эпидемиологии питания. Например, фрукты и овощи, потребляемые в Италии или на юге Европы, в целом импортируются из других стран лишь в незначительной доле, что сокращает расстояние между районом производства и розничными рынками, продолжительность хранения и степень использования пестицидов . Точно так же молочные продукты, потребляемые в США, отличаются от тех, что потребляются в Европе, методы производства, а также количество жира в готовых продуктах сильно различаются . Это может частично объяснить противоречивые результаты, связанные с потреблением овощей и фруктов или молочных продуктов, при сравнении итальянского исследования Parazzini и соавт. и американского исследования Trabert и соавт. . Кроме того, традиционно средиземноморская диета включает оливковое масло в больших количествах, чем типичная североамериканская диета, в то время как очень высокие уровни потребления мяса и сахара распространены в США . Эти различия могут повлиять на сопоставимость результатов исследований, проведенных в разных странах. Кроме того, может быть трудно выделить отдельные эффекты отдельных продуктов питания . Оливковое масло является основным заправочным жиром для овощей в соответствии со средиземноморской традицией . В большинстве исследований диета оценивалась с помощью опросников частоты приема пищи, которые характеризуются некоторой слабостью. Показатели частоты потребления пищевых продуктов ограничены в своей способности собирать сложную информацию из-за практических ограничений, присущих печатным форматам опросников. В частности, они представляют собой среднее количество приемов пищи, собранных в разные сезоны, и периоды с ограниченной информацией о размерах порций и способах приготовления пищи. Эти критические замечания можно применить, например, к Parazzini и соавт. . Были предложены некоторые стратегии для новой эпидемиологической практики в крупных когортных исследованиях. Эти стратегии включают в себя возможность использования преимуществ современных технологий для повышения достоверности диетической оценки или использования многодневных продовольственных записей . Однако в контексте эндометриоза, при котором обычно проходит много лет между появлением симптомов и окончательным диагнозом, применение этих перспективных стратегий представляется очень трудным.
Было показано, что диагноз эндометриоза чаще встречается среди женщин более высокого социального класса и более образованных , которые могли бы уделять больше внимания незначительным проблемам со здоровьем, но также могли бы иметь более ориентированное на здоровье отношение к диете и привычкам образа жизни. Более пристальное внимание к здоровью может способствовать диагностике эндометриоза, что приводит к неправильной оценке реальной связи с факторами питания. Только два исследования из числа выявленных были скорректированы с учетом факторов, связанных с социальным статусом.
Другой основной методологической проблемой в эпидемиологии питания является оценка влияния конкретных компонентов рациона с постоянными калориями (например, большее потребление красного мяса означает, что что-то еще в рационе должно быть уменьшено, например фрукты или овощи) или, если калории не поддерживаются постоянными, необходимо установить, как и в какой степени это может повлиять (например, большее потребление красного мяса означает не уменьшение чего-то еще, а скорее дополнительный/больший источник пищи). Все эти аспекты не были последовательно проанализированы в опубликованных работах. Несколько предыдущих исследований показали обратную зависимость между риском эндометриоза и индексом массы тела . По этой причине поправка на общее потребление энергии может иметь решающее значение, но очень немногие исследования обеспечили эту поправку. В целом различные методы корректировки, используемые в различных исследованиях, могут объяснить некоторые несоответствия, наблюдаемые в сообщаемых результатах. Выделенные популяции потенциальных предубеждений также могут быть обусловлены различным выбором контрольных групп в рассматриваемых исследованиях. Некоторые исследования включали женщин с миомой матки или необъяснимым бесплодием в качестве контроля, и недавно было показано, что на эти состояния влияет потребление некоторых питательных веществ . Обратная связь между потреблением овощей и фруктов и риском развития ряда заболеваний является одним из наиболее распространенных факторов в диетической эпидемиологии . В двух исследованиях была проанализирована связь между потреблением зеленых овощей и фруктов в неделю или день и риском развития эндометриоза . В итальянском исследовании «случай-контроль» потребление зеленых овощей и фруктов было обратно связано с риском развития эндометриоза .
Данные анализировались с учетом количества порций в неделю. Значительное снижение риска возникло при высоком потреблении зеленых овощей и свежих фруктов. Ассоциации были в целом последовательными даже после корректировки на смешивающие факторы. В исследовании «случай-контроль», проведенном Trabert и соавт. , роль диеты, богатой зелеными овощами и фруктами, была проанализирована с учетом количества порций в день аналогично итальянскому исследованию «случай-контроль». Увеличение количества порций фруктов в день ассоциировалось с повышенным риском заболевания (две или более против одной или менее порций в день), но никакой ассоциации с овощами не возникало . Интересно, что овощи (в частности, зеленые овощи) содержат фолаты, метионин и витамин В6, которые участвуют в «питательной геномике» . Критическим в этом контексте является группа питательных веществ, обычно называемых липотропами, которая включает метионин, холин, фолиевую кислоту и витамин В6, которые могут воздействовать на геном человека, изменяя экспрессию генов или генных продуктов, и могут влиять на метилирование ДНК . Все составы «липогенных метил-дефицитных диет» (т. е. дефициты холина, метионина-холина или метионин-холина-фолиевой кислоты) провоцируют ряд сходных молекулярных изменений, включая изменение липидного обмена, окислительный стресс и ряд эпигенетических нарушений, которые могут привести к прогрессирующему повреждению тканей, способствующему развитию первичных опухолей . На самом деле эпигенетические аномалии и аберрантные паттерны ДНК-метилирования также предполагаются вовлеченными в эндометриоз . С другой стороны, овощи, но особенно фрукты, могут содержать хлорорганические соединения , которые, в свою очередь, были положительно связаны с риском развития эндометриоза . В пяти из 10 исследований, посвященных липофильным химическим веществам окружающей среды и эндометриозу, у женщин с эндометриозом наблюдались значительно более высокие концентрации, чем у женщин без эндометриоза, но результаты не были последовательными . Хлорорганические соединения, как полагают, влияют на гормональные пути, поскольку они, как было показано, оказывают плейотропные эффекты через эстрогенные и андрогенные рецепторы . Необходимы дополнительные данные, чтобы выяснить, может ли развитие эндометриоза зависеть от таких питательных веществ, как овощи, которые поставляют или регенерируют метильные группы. Точно так же, поскольку невозможно сделать какие-либо выводы из связи между потреблением фруктов и эндометриозом, влияние воздействия хлорорганических соединений на развитие эндометриоза через прием загрязненных пищевых продуктов остается неясным. В четырех исследованиях конкретно рассматривалась роль отдельных микроэлементов, содержащихся в овощах и фруктах, в частности фолатов, каротиноидов и витаминов А, Е и С, в риске развития эндометриоза .
Фолаты
Не выявлено ассоциации между потреблением фолатов и риском развития эндометриоидных кист яичников в исследованиях «случай-контроль», в том числе 280 случаев таких кист . Аналогично, Traber и соавт. не обнаружили статистической связи между эндометриозом и общим потреблением фолатов , и в том же исследовании не было обнаружено никакой связи между потреблением витаминов В6, В12 и ниацина. Витамин А присутствует только в продуктах животного происхождения, таких как печень, почки, жирная рыба и молочные продукты, но также может быть преобразован эндогенно из своего пищевого предшественника β-каротина, содержащегося в основном в зеленых листовых и желтых овощах и оранжевых фруктах. Таким образом, провитамины А (каротиноиды) из растений являются дополнительным основным диетическим источником витамина А для большинства населения мира . В целом потребление β-каротина или витамина А статистически не ассоциировано с риском развития эндометриоза . В итальянском исследовании потребление печени или моркови, двух важных источников витамина А, было проанализировано в связи с риском развития эндометриоза и не было выявлено никакой связи с потреблением печени, хотя число субъектов, сообщивших о потреблении печени, было низким. Что касается моркови, то представленные данные о потенциальном снижении риска были неоднозначными . Потребление витамина А было значительно ниже у пациенток с эндометриозом в исследовании Mier-Cabrera и соавт. . Потребление витамина А составило 110 ± 23% от рекомендуемой суточной нормы потребления у пациенток с эндометриозом по сравнению с 163 ± 45% в контроле (p < 0,05) . Данные о витаминах С и Е также противоречивы. Прием витамина С и витамина Е не был связан с риском развития эндометриоза в трех исследованиях . В исследовании Mier-Cabrera и соавт. было продемонстрировано более низкое потребление витаминов С и Е у пациенток с эндометриозом.
Потенциальная биологическая связь между витаминами и эндометриозом
Витамины, в частности С и Е, оказывают мощное антиоксидантное действие на перекисное окисление липидов (ПОЛ). Цепная реакция ПОЛ может быть инициирована многими активными формами кислорода (АФК), производимыми различными источниками. ПОЛ способствует развитию и прогрессированию хронических заболеваний с воспалительным компонентом . Кроме того, была также описана новая роль АФК как второго мессенджера клеточной пролиферации, поскольку нормальная клеточная пролиферация коррелировала с продукцией эндогенных АФК через активацию связанных с ростом сигнальных путей, включая активированную митогеном протеинкиназу ERK1/2 . Эти наблюдения ставят вопрос о том, существует ли причинно-следственная связь между окислительным стрессом и заболеванием. Если это так, то антиоксидантная терапия должна оказаться полезной при хронических воспалительных и пролиферативных заболеваниях . Установлено также, что маркеры окислительного стресса повышены в сыворотке крови и перитонеальной жидкости больных эндометриозом . Известная корреляция между АФК и пролиферацией клеток, наряду с повышенной продукцией АФК в ответ на хроническое воспаление при эндометриозе, предположила возможную роль АФК в регуляции пролиферации эндометриотических клеток. На самом деле эндометриоидная клеточная пролиферация и активация ERK1/2 отменяются молекулой антиоксиданта N-ацетилцистеина как in vitro, так и в мышиной модели эндометриоза . В соответствии с этими наблюдениями Миер-Кабрера и др. исследовали действие высокоокислительной диеты (витамины А, С и Е) у пациенток с эндометриозом в течение 4 месяцев и показали положительный эффект за счет уменьшения маркеров окислительного стресса и улучшения активности антиоксидантных ферментов и концентрации витаминов в периферической крови. Эти эффекты не наблюдались у женщин, получавших контрольную диету . Наконец, возможно, что антиоксидантное действие витаминов может уменьшить клинические последствия эндометриоза. Окислительный стресс также был связан с бесплодием . Однако в рандомизированном плацебо-контролируемом клиническом исследовании, включавшем 44 женщины с эндометриозом, влияние на фертильность батончика, содержащего витамины С и Е (343 и 84 мг/сут соответственно), даваемого в течение 6 месяцев, было сопоставлено с плацебо, и никакого эффекта не возникло, поскольку частота беременности составила 19% в группе витаминов и 12% в группе плацебо . Взаимосвязь между потреблением пищевых жиров и риском развития эндометриоза была проанализирована в пяти исследованиях «случай-контроль» и в когортном исследовании. Результаты, полученные в отношении общего потребления жиров, плохо определены , поэтому различные типы жиров и различные жиросодержащие продукты будут рассмотрены для того, чтобы лучше рассмотреть эту конкретную тему.
Красное мясо и насыщенные жиры
В трех исследованиях был проведен анализ риска развития эндометриоза в зависимости от количества порций мяса в неделю или потребления сливочного масла , которые считаются основными источниками насыщенных жиров. В итальянском исследовании «случай-контроль» риск эндометриоза был значительно выше у женщин, сообщавших о более высоком потреблении мяса и ветчины. Однако не выявлено никаких взаимосвязей с приемом масла . В бельгийском клиническом исследовании «случай-контроль» потребление сливочного масла, но не мяса было незначительно связано с риском перитонеального эндометриоза в нескорректированном анализе . В исследовании «случай-контроль», проведенном Trabert и соавт. , не было выявлено связи между риском развития эндометриоза и количеством порций красного мяса в неделю . Насыщенные жиры и животные жиры не были достоверно связаны с риском развития эндометриоза в исследованиях, посвященных конкретным питательным веществам . Однако этот аспект нуждается в дальнейшем изучении, учитывая, что диета, характеризующаяся высоким потреблением красного мяса, умеренно связана с концентрациями эстрадиола и эстрона сульфата , и, как следствие, его потребление может непосредственно влиять на концентрацию циркулирующих стероидных гормонов в организме человека и, в конечном счете, на поддержание заболевания.
Оливковое масло и мононенасыщенные жиры
Оливковое масло является основным источником мононенасыщенных жиров в средиземноморских странах. Другие источники мононенасыщенных жиров включают красное мясо, цельные молочные продукты, орехи, сало, кунжутное масло, кукурузное масло, попкорн, цельнозерновые и пшеничные злаки. В итальянском исследовании «случай-контроль» не было выявлено связи между потреблением масла и риском развития эндометриоза . Аналогично, в исследовании Nurses’ Health Study II не было выявлено связи между потреблением мононенасыщенных жиров или растительных жиров и риском развития эндометриоза . В исследовании Britton и соавт. женщины в самых высоких квартилях потребления мононенасыщенных жиров имели более высокий риск развития эндометриоидных кист яичников, хотя риск стал незначительным после корректировки на потребление полиненасыщенных жиров. С другой стороны, повышенный риск наблюдался при высоком потреблении растительных жиров даже после корректировки на потребление полиненасыщенных жиров . Оливковое масло является важным источником микроэлементов и широкого спектра ценных антиоксидантов, которые не содержатся в других маслах . Высокое содержание олеиновой кислоты делает оливковое масло гораздо менее подверженным окислению, чем, например, полиненасыщенные жирные кислоты (ПНЖК). Кроме того, в оливковом масле большинство репрезентативных фенолов считаются мощными поглотителями супероксида и других активных веществ . С другой стороны, иммуносупрессивные эффекты, связанные с диетой с оливковым маслом, не так велики, как эффекты, производимые длинноцепочечными омега-3 ПНЖК, которые считаются наиболее иммуносупрессивными жирными кислотами . Связь между потреблением мононенасыщенных жиров и эндометриозом еще предстоит установить.
Рыба и омега-3 ПНЖК
Полиненасыщенные жиры содержатся в основном в орехах, семенах, рыбе, водорослях, листовой зелени и криле. В итальянских и бельгийских исследованиях не было обнаружено статистической связи между потреблением рыбы и эндометриозом, хотя тенденция к снижению риска могла наблюдаться у Parazzini и соавт. и Heilier и соавт. , в то время как полное отсутствие какой-либо ассоциации было обнаружено Trabert и соавт. . В исследовании Nurses’ Health Study II не выявлено взаимосвязи с потреблением жиров. Интересно, что авторы объяснили эту потенциальную ассоциацию с точки зрения влияния витамина D и кальция на механизмы, способствующие развитию заболевания. Кроме того, в том же исследовании сообщалось о снижении, но не значительном, риска развития эндометриоза, связанного с повышенным потреблением витамина D и кальция. Интригующее объяснение связи между эндометриозом и витамином D может быть получено из наблюдения, что витамин D стимулирует регуляторные Т-клетки и секрецию интерлейкина-10 (ИЛ-10), снижает концентрацию провоспалительного цитокина ИЛ-17 и ослабляет иммунную функцию T-хелперов 1-го типа . Таким образом, дефицит витамина D может быть выявлен как биологически вероятный путь к увеличению риска воспалительных заболеваний , и это объяснение может также относиться к эндометриозу. Однако в двух исследованиях, в том числе в одном из этой группы, не удалось обнаружить более низких концентраций витамина D у женщин с эндометриозом . В связи с этим в итальянских и бельгийских исследованиях не было отмечено связи между потреблением молока и сыра и риском развития эндометриоза . В трех исследованиях сообщалось о повышенном риске у женщин, сообщавших о любом или нечастом потреблении кофе с эндометриозом . Взаимосвязь была статистически значимой в двух случаях . Потребление кофеина и напитков, содержащих кофеин, положительно связано с концентрацией глобулинов, связывающих половые гормоны, и обратно с биодоступным тестостероном . Однако было обнаружено, что концентрация эстрогенов ранней фолликулярной фазы и концентрация эстрона выше у женщин с высоким потреблением кофеина . Эти гормональные изменения могут влиять на гормонозависимые заболевания. Однако ограниченные данные не дают возможности сделать какой-либо вывод о связи между употреблением кофе и риском развития эндометриоза.
Волокна, цельные и рафинированные злаки
В трех исследованиях конкретно рассматривалась связь между потреблением клетчатки и риском развития эндометриоза . В исследовании Traber и соавт. , медиана суточного потребления клетчатки составила 13,9 г в случаях и 14,7 г в контроле, и разница не была существенной . Потребление сырой клетчатки не было связано с риском развития эндометриоза в исследовании Britton и соавт. . С другой стороны, Savaris и do Amaral обнаружили статистически более высокое потребление волокон при эндометриозе. Аналогично, в итальянском исследовании «случай-контроль» не было выявлено связи между потреблением цельнозерновой пищи и риском развития эндометриоза . Диеты, богатые клетчаткой, повышают экскрецию эстрогенов и снижают биодоступность эстрогенов , в то время как рафинированные и цельнозерновые злаки влияют на гликемический индекс и гликемическую нагрузку, переменные, которые измеряют скорость всасывания углеводов и, следовательно, потребность в инсулине. Было показано, что инсулин способен стимулировать пролиферацию стромальных клеток эндометрия, связываясь с его рецепторами в эндометрии. Кроме того, гиперинсулинемия может повышать концентрацию эстрогенов за счет снижения концентрации глобулина, связывающего половые гормоны, и может повышать концентрацию инсулиноподобного фактора роста 1 за счет снижения концентрации инсулиноподобного фактора роста, связывающего белок I. Как эстрогены, так и инсулиноподобный фактор роста 1 стимулируют пролиферацию эндометриальных клеток . Исходя из этих наблюдений, потребление клетчатки и зерновых может быть связано с риском развития эндометриоза. Однако опубликованные данные не убедительно подтверждают эту взаимосвязь. Потребление сои и фитоэстрогенов распространено в Японии и в Юго-Восточной Азии в целом. Принимая во внимание связь между эндометриозом и эстрогенами, можно предположить, что потребление сои или, в целом, фитоэстрогенов может быть связано с риском заболевания. В единственном исследовании, проведенном в Японии, эта связь была изучена. Более высокие концентрации генистеина и дайдзеина в моче ассоциировались со снижением риска развития прогрессирующего, но не минимально легкой стадии эндометриоза у бесплодных женщин . Соя богата фитоэстрогенами, которые из-за их слабого эстрогенного и антиэстрогенного действия были связаны с риском заболеваний, связанных с эстрогенами . Как генистеин, так и пуэрарин были испытаны на животных моделях эндометриоза, где было показано, что они уменьшают массу и площадь поверхности эндометриотических поражений за счет ингибирования экспрессии ароматазы и экстрогенового рецептора-α (ЭРα) и снижения концентрации эстрогена . Однако эти открытия требуют подтверждения на людях.
На основании данного обзора литературы относительно связи между потреблением отдельных диетических факторов и риском развития эндометриоза, можно суммарно сделать несколько выводов. Несколько книг и веб-сайтов недавно были посвящены защитному или, наоборот, вредному влиянию диетических факторов на риск развития эндометриоза . Однако из представленных здесь выводов видно, что данная тема характеризуется крайней скудостью научных данных и крайней изменчивостью полученных результатов. Выводы о роли овощей, фруктов, красного мяса, витаминов в целом, молочных продуктов, кофе и ненасыщенных жиров противоречивы. Были предложены некоторые биологические механизмы, подтверждающие роль всех этих диетических факторов во влиянии на риск эндометриоза, но эпидемиологические данные не всегда подтверждают эти гипотезы. Основываясь на скудости научных данных, это исследование подробно описывает результаты нескольких исследований, чтобы подчеркнуть даже небольшие эффекты, но, учитывая очевидные несоответствия в сообщаемых результатах, сильная или убедительная информация не может быть предоставлена. Этот обзор мог бы стать исходной платформой для дальнейших исследований, направленных на изучение этих факторов. В настоящем обзоре подчеркиваются важнейшие аспекты исследований, проведенных до настоящего времени, с тем, чтобы укрепить идею о необходимости проведения дополнительных исследований. В этом обзоре также подчеркивается идея о том, что эндометриоз — это многоступенчатый феномен, в котором фаза становления заболевания сопровождается пролиферацией, васкуляризацией и перитонеальной инвазией эндометриотических очагов с сопутствующим проявлением воспалительной реакции. Различные питательные вещества могут оказывать различное воздействие на различные стадии развития болезни. Дальнейшие исследования могут отдельно проанализировать роль диеты в развитии или клинических последствиях эндометриоза. В заключение следует отметить, что, несмотря на противоречивые результаты немногочисленных эпидемиологических исследований, последствия для общественного здравоохранения и биологическая достоверность благоприятного воздействия некоторых питательных веществ на течение эндометриоза свидетельствуют о необходимости проведения дальнейших исследований в этой области.
Работа выполнена при финансовой поддержке гранта РНФ: конкурс 2018 г. «Проведение фундаментальных научных исследований и поисковых научных исследований отдельными научными группами», название проекта «Современные клинико-морфологические и иммунобиологические аспекты генитального эндометриоза», номер проекта 18-15-00165.
Литература
Л. В. Адамян, доктор медицинских наук, профессор, академик РАН
К. Н. Арсланян, кандидат медицинских наук
О. Н. Логинова¹, кандидат медицинских наук
Э. И. Харченко, кандидат медицинских наук
ФГБОУ ВО МГМСУ им. А. И. Евдокимова, Москва
¹ Контактная информация: poddubnay@yandex.ru




